
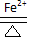 2PbSO4+2H2O��
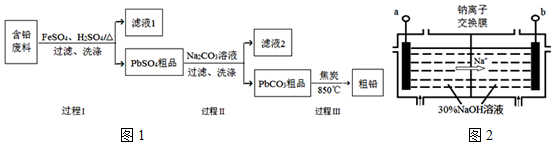
2PbSO4+2H2O������ �ԷϾ�Ǧ�����еĺ�Ǧ���ϣ�Pb��PbO��PbO2��PbSO4��̿�ڵȣ�Ϊԭ�ϣ��Ʊ���Ǧ����Ǧ���ϼ�������������ϡ������ȷ�Ӧ���˵õ�PbSO4��Ʒ������̼������Һ���˵õ�PbCO3��Ʒ�������м��뽹̿��850������Ǧ��
��1����1�����������ѧ��������֪�����̢��У���Fe2+���£�Pb��PbO2��H2SO4��Ӧ����PbSO4��ˮ��
��2���ٴ���ͨ���μӷ�Ӧ���ı䷴Ӧ���̣����ͷ�Ӧ�Ļ�ܣ��ӿ컯ѧ��Ӧ���ʣ��������������ͻ�ѧ���ʷ�Ӧǰ�ֲ��䣮���������Ϣ֪��Ӧi��Fe2+��PbO2����ΪFe3+����Ӧii��Fe3+��Pb��ԭΪFe2+���ݴ���д���ӷ���ʽ��
��aʵ��֤��������Ӧi����bʵ����֤��������Ӧii��ʵ�鷽��Ϊȡa�к�ɫ��Һ�������������Pb����ַ�Ӧ��ɫ��ȥ��
��3����ΪKsp��PbSO4��=1.6��10-5��Ksp ��PbCO3��=3.3��10-14��c��SO42-��=1.6mol•L-1��c��CO32-��=0.1mol•L-1��PbCO3�У�c��Pb2+��=$\frac{KsP��PbC{O}_{3}��}{c��C{{O}_{3}}^{2-}��}$=$\frac{3.3��1{0}^{-14}}{0.1}$=3.3��10-13����PbSO4�У�Q=c��Pb2+����c��SO42-��=3.3��10-13��1.6=5.28��10-13��Ksp��PbSO4����˵��PbSO4��ĸҺ��δ���ͣ���PbCO3�в�����PbSO4��
��4���ٸ����������������ƶ�֪��aΪ���������Դ����������
�ڵ������У�PbO2�������õ��ӣ��缫��ӦʽΪPbO2+4e-+2H2O=Pb+4OH-��
�������ӽ���Ĥֻ����������ͨ������ֹHPbO2-���������ұ��������Ӷ����PbԪ�ص������ʣ�
��� �⣺��1�����������ѧ��������֪�����̢��У��ڴ��£�Pb��PbO2��H2SO4��Ӧ����PbSO4��ˮ����ѧ����ʽΪ��Pb+PbO2+2H2SO4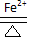 2PbSO4+2H2O��
2PbSO4+2H2O��
�ʴ�Ϊ��Pb+PbO2+2H2SO4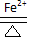 2PbSO4+2H2O��
2PbSO4+2H2O��
��2���ٴ���ͨ���μӷ�Ӧ���ı䷴Ӧ���̣����ͷ�Ӧ�Ļ�ܣ��ӿ컯ѧ��Ӧ���ʣ��������������ͻ�ѧ���ʷ�Ӧǰ�ֲ��䣮���������Ϣ֪��Ӧi��Fe2+��PbO2����ΪFe3+����Ӧii��Fe3+��Pb��ԭΪFe2+�����ӷ���ʽΪ��2Fe3++Pb+SO42-�TPbSO4+2Fe2+��
�ʴ�Ϊ��2Fe3++Pb+SO42-�TPbSO4+2Fe2+��
��aʵ��֤��������Ӧi����bʵ����֤��������Ӧii��ʵ�鷽��Ϊ��
a�����ữ��FeSO4��Һ�м���KSCN��Һ����Һ������ɫ���ټ�������PbO2����Һ��죬�������ӱ�����Ϊ�����ӣ�
b��ȡa�к�ɫ��Һ��������Һ�д���ƽ�⣬Fe3++3SCN-=Fe��SCN��3���������Pb����ƽ��״̬�������ӷ�Ӧ�����������ӣ�ƽ��������г�ַ�Ӧ��ɫ��ȥ��
�ʴ�Ϊ��ȡa�к�ɫ��Һ��������������Pb����ַ�Ӧ��ɫ��ȥ��
��3����ΪKsp��PbSO4��=1.6��10-5��Ksp ��PbCO3��=3.3��10-14��c��SO42-��=1.6mol•L-1��c��CO32-��=0.1mol•L-1��PbCO3�У�c��Pb2+��=$\frac{KsP��PbC{O}_{3}��}{c��C{{O}_{3}}^{2-}��}$=$\frac{3.3��1{0}^{-14}}{0.1}$=3.3��10-13����PbSO4�У�Q=c��Pb2+����c��SO42-��=3.3��10-13��1.6=5.28��10-13��Ksp��PbSO4����˵��PbSO4��ĸҺ��δ���ͣ���PbCO3�в�����PbSO4��
�ʴ�Ϊ����
��4���ٸ����������������ƶ�֪��aΪ���������Դ����������
�ʴ�Ϊ������
�ڵ������У�PbO2�������õ��ӣ��缫��ӦʽΪPbO2+4e-+2H2O=Pb+4OH-��
�ʴ�Ϊ��PbO2+4e-+2H2O=Pb+4OH-��
�������ӽ���Ĥֻ����������ͨ������ֹHPbO2-���������ұ��������Ӷ����PbԪ�ص������ʣ�
�ʴ�Ϊ����ֹHPbO2-���������ұ�������
���� ���⿼��δ֪��Ӧ��д���ܶȻ����绯ѧ������ʵ�����⣬�Ǹ߿��������ͣ�����չʾ���û�ѧ֪ʶ������������е�ʵ�����⣬��Ŀ�ѶȽϴ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ag+��Ag | B�� | Fe3+��Fe2+ | C�� | H+��H2 | D�� | Fe��OH��2��Fe��OH��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.15 mol•L-1 | B�� | 0.225 mol•L-1 | C�� | 0.30 mol•L-1 | D�� | 0.45 mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2O���ڼ��������� | |
| B�� | Na2CO3���ڱ�¶�ڿ����б�ΪNaHCO3 | |
| C�� | NaOH��Һ�����ڴ��������IJ���ƿ�� | |
| D�� | ��NaHCO3��Һ�еμ�ϡ���ᣬ��ʼʱ������һ��ʱ��������ݲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����£���1L1mol•L-1Na2SO3��Һ����SO2ʱ����ҺpH��SO2�����ʵ����ı仯��ͼ��ʾ������˵����ȷ���ǣ�������
�����£���1L1mol•L-1Na2SO3��Һ����SO2ʱ����ҺpH��SO2�����ʵ����ı仯��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | Na2SO3��Һ�У�c��Na+����c��SO32-����c��HSO3-����c��OH-����c��H+�� | |
| B�� | ������Һ������ʱ��c��Na+��=c��HSO3-��+2c��SO32-�� | |
| C�� | M ��ʱ��Һ�У�c��SO32-����c��HSO3-�� | |
| D�� | ��N�������Һ�м�ˮ��ʹ��Һ��pH��6.2���ߵ�7.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NF3���ӵĿռ乹��Ϊ������ | |
| B�� | �����ᣨHN3����һ�����ᣬ�ɲ��ֵ����H+��N3-����N2O��N3-��Ϊ�ȵ����� | |
| C�� | ����������Co3+���γ������磺[Co��N3����NH3��5]SO4���������ܵ���λ��Ϊ8 | |
| D�� | NaN3��KN3�Ľṹ���ƣ���NaN3�ľ����ܴ���KN3�ľ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H+��Ca2+��NO3-��CO32- | B�� | K+��Na+��Cl-��SO42- | ||
| C�� | Ag+��Na+��Cl-��K+ | D�� | NH4+��K+��OH-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
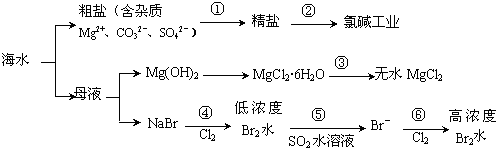
| A�� | ���̢ٵ��ᴿ���������̣����̢�ͨ��������ԭ��Ӧ�ɲ���2�ֵ��� | |
| B�� | �ڹ��̢��н�MgCl2•6H2O���ռ����Ƶ���ˮMgCl2 | |
| C�� | ���̢ݷ�Ӧ����Һ��ǿ���ԣ���������������豸�ĸ�ʴ���� | |
| D�� | �ڹ��̢ܡ���Ӧ��ÿ����0.2 mol Br- ������2.24 L Cl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com