
设NA表示阿伏加德罗常数的值,下列叙述中不正确的是:
A.常温常压下,1mol甲基(-CH3)含有的电子数为9NA
B.1 mol FeCl3跟水完全反应转化为氢氧化铁胶体后胶体粒子的数目小于NA
C.标况下,2.24LHF中含有的电子数为NA
D.1 mol 金刚砂(SiC)中含有4NA碳硅键
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、为加快反应速率,缩短达到平衡所需要的时间 |
| B、加快正反应速率,减小逆反应速率 |
| C、使平衡向合成氨的方向移动 |
| D、提高原料转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,pH=13的氨水中含有OH-的数目为0.1NA | B、1mol Na被完全氧化生成Na2O2,转移电子的数目为NA | C、标准状况下,2.24L NO2与水反应生成NO3-的数目为0.1NA | D、4.0g H2与足量N2完全反应生成NH3,反应中断裂共价键的总数为2NA |
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市房山区下学期高二期末测验化学试卷(解析版) 题型:选择题
某原电池装置如下图所示。下列有关叙述中,正确的是
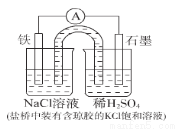
A.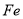 作正极,发生氧化反应 B. 工作一段时间后,两烧杯中溶解
作正极,发生氧化反应 B. 工作一段时间后,两烧杯中溶解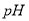 均不变
均不变
C.负极反应: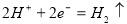 D. 工作一段时间后,NaCl溶液中c(Cl-)增大
D. 工作一段时间后,NaCl溶液中c(Cl-)增大
查看答案和解析>>
科目:高中化学 来源:2014~2015学年重庆市9月月考高一化学试卷(解析版) 题型:实验题
(14分)某实验小组用0.50 mol·L- 1 NaOH溶液和0.50mol·L- 1 的硫酸溶液进行中和热的测定。
 Ⅰ.配制0.50mol·L- 1 硫酸溶液
Ⅰ.配制0.50mol·L- 1 硫酸溶液
(1)若配制250 mL硫酸溶液,则须用量筒量取密度为1.84 g·cm- 3、质量分数为98%的浓硫酸 mL。
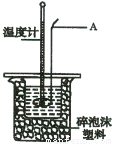
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如右图所示:
(2)仪器A的名称为 ;
(3)装置中碎泡沫塑料的作用是 ;
(4)写出该反应中和热的热化学方程式:(中和热为57.3 kJ·mol- 1) ;
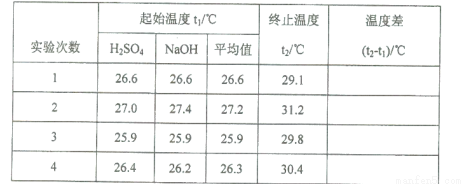
(5)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①下表中的温度差平均值为 ℃;
②近似认为0.50mol·L- 1 NaOH溶液和0.50mol·L- 1 硫酸溶液的密度都是1g·cm- 3 ,中和后生成溶液的比热容c= 4.18 J·(g·℃)- 1 。则中和热△H= (取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol- 1 有偏差,产生此实验偏差的原因可能是(填字母) 。
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.一次性把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源:2014~2015学年江苏省高二(文)上学期期中化学试卷(解析版) 题型:填空题
(15分)本题为选做题,包括A、B两题。选学《化学与生活》模块的考生答A题,选学《有机化学基础》模块的考生答B题,每位考生只可选做1题。若两题都作答,则以A题计分。
A.《化学与生活》生活中处处有化学。
(1)合理选择饮食、正确使用药物是保证身心健康的重要方面,请填写下列空格。
①维生素C能促进人体生长发育。下列富含维生素C的是 (填字母)。
A.牛肉 B.辣椒 C.鸡蛋
②缺乏某种微量元素将导致甲状腺肿大,且造成智力损害,该微量元素是
A.碘 B.铁 C.钙
③人体内蛋白质在蛋白酶作用下,水解为 ,在鸡蛋清溶液中加入饱和硫酸铵溶液有沉淀析出的过程称为 。
④使用青霉素可能会产生过敏,在用药前患者一定要进行 。
(2)材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础。请填写下列空格。
①生活中的 属于传统无机硅酸盐材料。(常见的三大类)
②合金材料钢铁里的Fe和C在潮湿的空气中因构成许多原电池而易发生电化学腐蚀,负极反应方程式为 。
③居室装修材料如化纤地毯、三合板等均会释放出污染空气的 气体。
④在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其各成分金属的熔点 。(选填“高”或“低”)
⑤现代以石油化工为基础的三大合成材料是 。
(3)保持洁净安全的生存环境已成为全人类的共识,人与自然要和谐相处。
①2013年,全国多个省市出现严重的雾霾天气。导致雾霾形成的主要污染物是 (填字母);
A.O2 B.CO2 C.PM2.5
②pH< 的雨水称为酸雨;向煤中加入适量的 ,可以大大减少燃物产物中SO2的量。
③在处理的废水时,需先加入明矾,明矾起净水作用的离子方程式为 。
④漂白粉可用于生活用水的杀菌消毒,工业上利用氯气和石灰乳制取漂白粉的化学反应方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014~2015学年江苏省高二(文)上学期期中化学试卷(解析版) 题型:选择题
在强酸性溶液中,可以大量共存的离子组是
A.Al3+、Na+、SO42- B.K+、NO3-、CO32-
C.Na+、HCO3-、Cl﹣ D.Ag+、Al3+、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com