
| A. | Pt | B. | Cu | C. | A1 | D. | Ag |
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:实验题
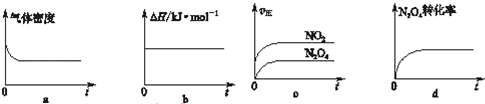
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
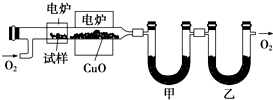
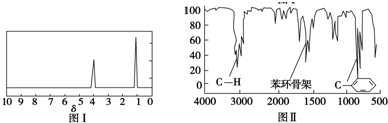
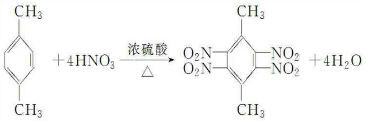 .
.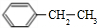 、
、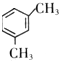 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧瓶必须垫石棉网加热 | |
| B. | 冷凝管中的水流是从下口进入,上口排出 | |
| C. | 实验中需要在烧瓶中加入几粒碎瓷片,防止出现暴沸现象 | |
| D. | 温度计的水银球应插入烧瓶中的液面以下 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KNO3和K2O都属于盐 | B. | KOH和Na2CO3都属于碱 | ||
| C. | H2SO3和HNO3都属于酸 | D. | CaO和Na2SO4都属于氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二上10月月考化学卷(解析版) 题型:选择题
下列关于反应热的说法正确的是
A.已知C(石墨,s)=C(金刚石,s) △H>0,说明金刚石比石墨稳定
B.已知H+(aq)+OH-(aq)=H2O(l) △H=-57.4kJ/mol,则含20.0gNaOH的稀溶液与稀醋酸完全中和,放出热量小于28.7kJ
C.已知甲烷的燃烧热为890.3kJ/mol,则表示甲烷燃烧热的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ/mol
D.将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)  2NH3(g) △H=-38.6kJ/mol
2NH3(g) △H=-38.6kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com