
| A.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是: c[(NH4)2Fe(SO4)2] < c[(NH4)2SO4] < c(NH4Cl) |
| B.向AgCl悬浊液中滴入KI溶液,有AgI沉淀生成,说明AgCl的溶解度小于AgI的溶解度 |
| C.0.2 mol/L HCl溶液与等体积0.05 mol/L Ba(OH)2溶液混合后,溶液的pH=1 |
| D.0.2 mol/L的NaHCO3溶液中c(H+)+c(H2CO3)=c(CO32-)+c(OH-) |
科目:高中化学 来源:不详 题型:单选题
| A.a<b | B.a>b |
| C.a="b" | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.[NH4+]=[Na+]=[OH-]>[NH3·H2O] |
| B.[NH4+]=[Na+]>[NH3·H2O]>[OH-] |
| C.[NH4+]>[Na+]>[OH-]>[NH3·H2O] |
| D.[NH4+]>[Na+]>[NH3·H2O]>[OH-] |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.α1=α2>α3=α4 |
| B.α2=α4>α1=α3 |
| C.α1=α2=α3=α4 |
| D.α1=α3>α2=α4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.绿色变深 | B.变得更浅 |
| C.变黄绿色 | D.不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.H2Y在电离时:H2Y+H2O HY-+H3O+ HY-+H3O+ |
| B.在该盐的溶液中,离子浓度为:c(Na+)>c(HY-)>c(Y2-)>c(OH-)>c(H+) |
| C.在该盐的溶液中,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+) |
D.HY-水解方程式为:HY-+H2O Y2-+H3O+ Y2-+H3O+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4Cl:[Cl-]>[H+]>[NH+4]>[OH-] |
| B.Na2CO3:[Na+]>[CO32-]>[HCO3-]>[OH-]>[H+] |
| C.NaHCO3:[Na+]>[CO32-]>[HCO3-]>[OH-]>[H+] |
| D.(NH4)2SO4:[NH4+]>[SO42-]>[H+]>[OH-] |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
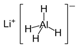 )、LiH是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是
)、LiH是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是| A.LiH与D2O反应,所得氢气的摩尔质量为4g/mol |
| B.1molLiAlH4在125℃完全分解,转移3mol电子 |
| C.LiAlH4溶于适量水得到无色溶液,则化学方程式可表示为:LiAlH4+2H2O=LiAlO2+4H2↑ |
| D.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com