
·ÖĪö £Ø1£©ÓÉÉŁĮæäå»ÆÄĘČÜŅŗµÄŹŌ¹ÜÖŠµĪ¼ÓÉŁĮæŠĀÖĘĀČĖ®£¬·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³Éä壬äåŅ×ČÜÓŚĖÄĀČ»ÆĢ¼£¬ĒŅŻĶČ”ŗóÓŠ»ś²ćŌŚĻĀ²ć£»
£Ø2£©äåĖ®æÉŃõ»ÆµāĄė×ÓÉś³Éµā£¬¼ÓĖÄĀČ»ÆĢ¼ŻĶČ”ŗóÓŠ»ś²ćŌŚĻĀ²ć£»
£Ø3£©ÓÉŃõ»Æ¼ĮµÄŃõ»ÆŠŌ“óÓŚŃõ»Æ²śĪļµÄŃõ»ÆŠŌÅŠ¶Ļ£»
£Ø4£©·śĘųĶØČėĀČ»ÆÄĘČÜŅŗÖŠ£¬·śĘųÓėĖ®·“Ӧɜ³ÉŃõĘų£®
½ā“š ½ā£ŗ£Ø1£©ÓÉÉŁĮæäå»ÆÄĘČÜŅŗµÄŹŌ¹ÜÖŠµĪ¼ÓÉŁĮæŠĀÖĘĀČĖ®£¬·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³Éä壬äåŅ×ČÜÓŚĖÄĀČ»ÆĢ¼£¬ĒŅŻĶČ”ŗóÓŠ»ś²ćŌŚĻĀ²ć£¬ŌņĻĀ²ć³Ź³ČÉ«£¬ÓŠ¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒCl2+2NaBr=2NaCl+Br2£¬ĘäÖŠµÄŃõ»Æ¼ĮŹĒCl2£¬
¹Ź“š°øĪŖ£ŗ³Č£»Cl2+2NaBr=2NaCl+Br2£»Cl2£»
£Ø2£©ĻņŹ¢ÓŠÉŁĮæµā»ÆÄʵďŌ¹ÜÖŠµĪ¼ÓÉŁĮæäåĖ®£¬Õńµ“£¬ŌŁ¼ÓČėĖÄĀČ»ÆĢ¼£¬Õńµ“ŗó¾²ÖĆ£®¹Ū²ģµ½ŅŗĢå·ÖĪŖĮ½²ć£¬ĻĀ²ć³Ź×ĻŗģÉ«£¬ÓÉ“ĖµĆ³öµÄ½įĀŪŹĒäåµÄŃõ»ÆŠŌĒæÓŚµā£¬
¹Ź“š°øĪŖ£ŗäåĖ®£»×Ļŗģ£»äåµÄŃõ»ÆŠŌĒæÓŚµā£»
£Ø3£©×ŪŗĻŅŌÉĻĮ½øöŹµŃ飬×īÖÕµĆ³öµÄ½įĀŪŹĒCl2”¢Br2”¢I2µÄŃõ»ÆŠŌŅĄ“Ī¼õČõ£¬
¹Ź“š°øĪŖ£ŗCl2”¢Br2”¢I2µÄŃõ»ÆŠŌŅĄ“Ī¼õČõ£»
£Ø4£©·śĘųĶØČėĀČ»ÆÄĘČÜŅŗÖŠ£¬Čō¹Ū²ģµ½ÓŠĘųÅŻĆ°³ö£¬²»ÄÜÖ¤Ć÷·śĘųµĆŃõ»ÆŠŌĒæÓŚĀČĘų£¬ĄķÓÉŹĒ·śĘųŌŚČÜŅŗÖŠ·¢Éś·“Ó¦ 2F2+2H2O=4HF+O2£¬ĖłŅŌ·śĘų²»ÄÜÖĆ»»³öĀČĘų£¬
¹Ź“š°øĪŖ£ŗ·śĘųŌŚČÜŅŗÖŠ·¢Éś·“Ó¦ 2F2+2H2O=4HF+O2£¬ĖłŅŌ·śĘų²»ÄÜÖĆ»»³öĀČĘų£®
µćĘĄ ±¾Ģāæ¼²éŠŌÖŹŹµŃé·½°øµÄÉč¼Ę£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕĀ±ĖŲµ„ÖŹµÄŃõ»ÆŠŌ±Č½Ļ”¢·śĘųµÄŠŌÖŹĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėŹµŃéÄÜĮ¦µÄ漲飬עŅāŃõ»Æ»¹Ō·“Ó¦µÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚŗ¬ÓŠµČĪļÖŹµÄĮæµÄAlO2-”¢OH-”¢CO32-ČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėŃĪĖį£ŗAlO2-”¢OH-”¢CO32- | |
| B£® | ŌŚŗ¬µČĪļÖŹµÄĮæµÄFeBr2”¢FeI2ČÜŅŗÖŠ£¬»ŗĀżĶØČėĀČĘų£ŗI-”¢Br-”¢Fe2+ | |
| C£® | ŌŚŗ¬µČĪļÖŹµÄĮæµÄKOH”¢Ba£ØOH£©2ČÜŅŗÖŠ£¬»ŗĀżĶØČėCO2£ŗKOH”¢Ba£ØOH£©2”¢K2CO3”¢BaCO3 | |
| D£® | ŌŚŗ¬µČĪļÖŹµÄĮæµÄFe3+”¢Cu2+”¢H+ČÜŅŗÖŠ¼ÓČėŠæ·Ū£ŗFe3+”¢Cu2+”¢H+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ū¢ß | B£® | ¢Ł¢Ü¢Ž | C£® | ¢Ś¢Ū¢Ž | D£® | ¢Ł¢Ü¢Ż¢ß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2 | B£® | CH4 | C£® | C2H4 | D£® | NH4Cl |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬7.8 gNa2O2ŗ¬ÓŠµÄNa+ŹżĪŖ0.2NA | |
| B£® | ±ź×¼×“æöĻĀ£¬22.4 LCl2ÓėĖ®³ä·Ö·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖNA | |
| C£® | ±ź×¼×“æöĻĀ£¬NAøöCO2ÓėSO2µÄ»ģŗĻĘųĢå·Ö×ÓÕ¼ÓŠµÄĢå»żŌ¼ĪŖ22.4 L | |
| D£® | 50”ę”¢1”Į105PaĻĀ6g NO2Óė0”ę”¢2”Į105 PaĻĀ46 g N2O4¾łŗ¬ÓŠ3NAøöŌ×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
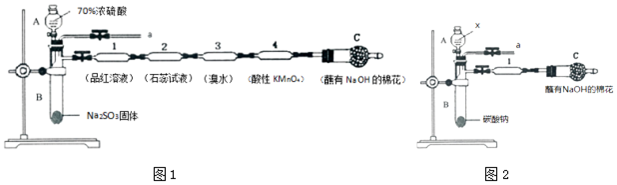
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
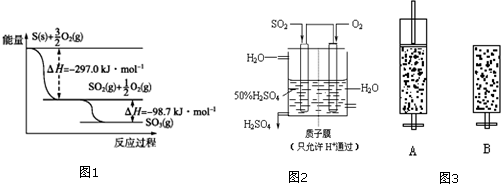
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
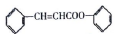 ŹĒŗĻ³Éøß¾Ū·Óõ„µÄŌĮĻ£¬ĘäŗĻ³ÉĀ·Ļߣزæ·Ö·“Ó¦Ģõ¼žĀŌČ„£©ČēĶ¼ĖłŹ¾£ŗ
ŹĒŗĻ³Éøß¾Ū·Óõ„µÄŌĮĻ£¬ĘäŗĻ³ÉĀ·Ļߣزæ·Ö·“Ó¦Ģõ¼žĀŌČ„£©ČēĶ¼ĖłŹ¾£ŗ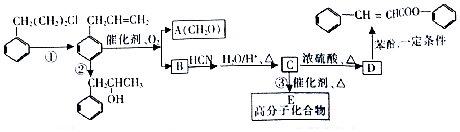
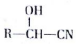 $”ś_{”÷}^{H_{2}O/H+}$
$”ś_{”÷}^{H_{2}O/H+}$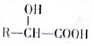
 $”ś_{”÷}^{“߻ƼĮ}$
$”ś_{”÷}^{“߻ƼĮ}$ +nH2O£®
+nH2O£® £ØČĪŠ“Ņ»ÖÖ£©£®
£ØČĪŠ“Ņ»ÖÖ£©£®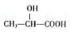 £©µÄĀ·ĻߣØĘäĖūŹŌ¼ĮČĪŃ”£¬ŗĻ³ÉĀ·Ļß³£ÓƵıķŹ¾·½Ź½ĪŖA$\stackrel{·“Ó¦ŹŌ¼Į}{”ś}$B”$\stackrel{·“Ó¦ŹŌ¼Į}{”ś}$Äæ±ź²śĪļ£©
£©µÄĀ·ĻߣØĘäĖūŹŌ¼ĮČĪŃ”£¬ŗĻ³ÉĀ·Ļß³£ÓƵıķŹ¾·½Ź½ĪŖA$\stackrel{·“Ó¦ŹŌ¼Į}{”ś}$B”$\stackrel{·“Ó¦ŹŌ¼Į}{”ś}$Äæ±ź²śĪļ£©²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com