
| A. | 向碳酸氢钙溶液中加过量氢氧化钠Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| B. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合Ba2++OH-+HCO3-═BaCO3↓+H2O | |
| C. | 氯化铝与过量氨水反应 Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 过量CO2通入氢氧化钡的稀溶液中 CO2+OH-═HCO3- |
分析 A.二者反应生成碳酸钙、碳酸钠和水;
B.等物质的量的氢氧化钡和碳酸氢铵反应生成碳酸钡、一水合氨和水;
C.氢氧化铝难溶于氨水;
D.过量二氧化碳和氢氧化钡反应生成可溶性碳酸氢钡.
解答 解:A.二者反应生成碳酸钙、碳酸钠和水,离子方程式为Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故A正确;
B.等物质的量的氢氧化钡和碳酸氢铵反应生成碳酸钡、一水合氨和水,离子方程式为Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3•H2O+H2O,故B错误;
C.氢氧化铝难溶于氨水,离子方程式为 Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故C正确;
D.过量二氧化碳和氢氧化钡反应生成可溶性碳酸氢钡,离子方程式为CO2+OH-═HCO3-,故D正确;
故选B.
点评 本题考查离子反应的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应及复分解反应的离子反应考查,易错选项是B.


科目:高中化学 来源: 题型:选择题
| A. | 化学是在原子、分子水平上研究物质的组成、结构、性质、制备等的自然科学 | |
| B. | 化学是一门具有创造性的科学,可以利用化学知识创造出自然界中不存在的物质 | |
| C. | 化学的发展经过了从宏观到微观,从感性到理性的逐步深化的过程 | |
| D. | 随着化学的发展,人们最终会实现通过化学变化使水变油的梦想 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 治疗胃酸过多,可用NaHCO3,不能用Al(OH)3,因其含有Al元素 | |
| B. | Al箔用砂纸打磨后,在空气中受热可以熔化,由于氧化膜被破坏,熔化的Al可以滴落 | |
| C. | 用铂丝做焰色反应实验,每次做完后都需要用盐酸洗涤,再灼烧至跟酒精灯火焰颜色相同后再使用 | |
| D. | 实验室制备Al(OH)3时,氨水不宜过量,因为Al(OH)3与过量的浓氨水反应生成NH4AlO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol固态焦炭与1mol水蒸气反应产生1mol一氧化碳和1mol氢气,吸收131.3 kJ的热量 | |
| B. | 碳与水反应吸收131.3 kJ的热量 | |
| C. | 1mol碳和1mol水反应吸收131.3 kJ的热量 | |
| D. | 固态碳和气态水各1mol反应,放出131.3 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,pH=5的NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| B. | 在0.1mol•L-1的CH3COONa溶液中:n(OH-)+0.1mol>n(CH3COOH)+n(H+)+n(Na+) | |
| C. | 向AgBr的饱和溶液中加入NaCl固体,有白色固体析出,说明AgCl比AgBr更难溶 | |
| D. | 10mL0.1mol•L-1H2SO4与10mL 0.01mol•L-1NaOH溶液充分混合,若混合后的体积为20mL,则溶液的pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
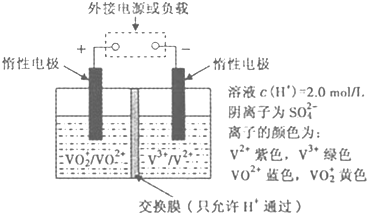
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com