
| A. | 不用铝片,改用铝粉 | B. | 不用稀硫酸,改用98%浓硫酸 | ||
| C. | 不用稀硫酸,改用浓硝酸 | D. | 加入少量稀盐酸 |
科目:高中化学 来源: 题型:解答题
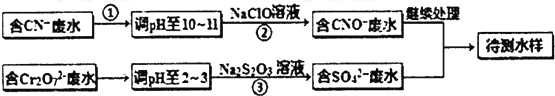
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸、氢氧化钠溶液能导电,所以它们都是电解质 | |
| B. | 电解质溶液通电时,电解质才能发生电离 | |
| C. | 水溶液能导电的化合物不一定是电解质 | |
| D. | 难溶物质肯定不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
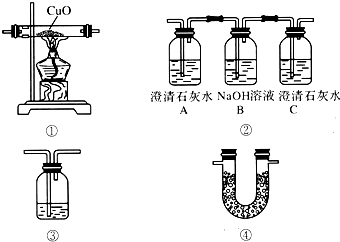
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 最外层电子数 | 次外层电子数 |
| D | x | x+4 |
| F | x+3 | x+4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是能起银镜反应的物质一定是醛 | |
| B. | 乙烯和甲苯都能使酸性高锰酸钾溶液褪色 | |
| C. | 酯在过量氢氧化钠溶液中水解生成的最终产物为酸和醇 | |
| D. | 苯酚有弱酸性,因此它是一种羧酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
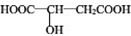 )常用于汽水、糖果的添加剂,
)常用于汽水、糖果的添加剂,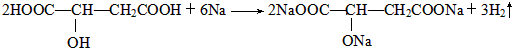 ;
;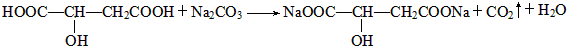
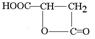 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用合适的催化剂可以增大反应速率 | |
| B. | 升高温度可以增大反应速率 | |
| C. | 增大压强不影响反应速率 | |
| D. | 增大N2浓度可以增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com