
下列物质中
①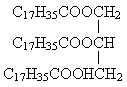 ②
②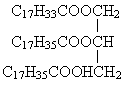
③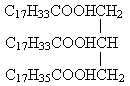 属于单甘油酯的是(填序号,下同)________,属于混甘油酯的是________.
属于单甘油酯的是(填序号,下同)________,属于混甘油酯的是________.
①发生皂化反应的化学方程式为________;
③发生氢化反应的化学方程式为________.
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 混 合 物 | 实验方案 | 反应化学方程式 | ||||||||
| (1)铁粉中混有少量铝粉 | 将混合物置于烧杯中,加入足量的NaOH溶液,反应后,过滤 将混合物置于烧杯中,加入足量的NaOH溶液,反应后,过滤 |
2Al+2NaOH+2H2O═2NaAlO2+3H2↑ 2Al+2NaOH+2H2O═2NaAlO2+3H2↑ | ||||||||
| (2)Na2CO3固体中混有少量NaHCO3 | 将混合物置于适当的容器中(如:试管、蒸发皿等),加热 将混合物置于适当的容器中(如:试管、蒸发皿等),加热 |
2NaHCO3
2NaHCO3
| ||||||||
| (3)FeCl3溶液中混有少量FeCl2 | 向该FeCl3溶液中通入适量的Cl2 向该FeCl3溶液中通入适量的Cl2 |
2FeCl2+Cl2=2FeCl3 2FeCl2+Cl2=2FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com