
已知:①A+B2+===A2++B ②D+2H2O===D(OH)2+H2↑ ③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-===E,B-2e-===B2+,下列说法正确的是
A.氧化性E2+>B2+>A2+>D2+
B.氧化性D2+>E2+>A2+>B2+
C.反应E+A2+===A+E2+能够进行
D.提取某废水中含有少量的A2+时可以选用D
 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
给下列有机物命名:
 ①麻黄素中含氧官能团的名称是________,属于______类(填“醇”或“酚”)。
①麻黄素中含氧官能团的名称是________,属于______类(填“醇”或“酚”)。
②下列各物质:
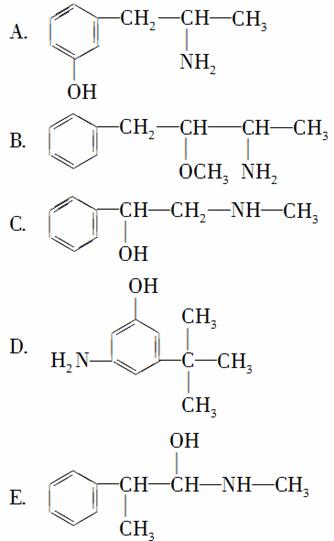
与麻黄素互为同分异构体的是________(填字母,下同),互为同系物的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
若甲烷与氯气以物质的量之比1:3混合,在光照下得到的产物:①CH3Cl②CH2Cl2③CHCl3④CCl4,其中正确的是
A.只有① B.只有② C.①②③的混合物 D.①②③④的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应属于区域3的是
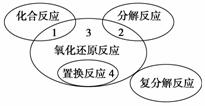
A.4Fe(OH)2+O2+2H2O===4Fe(OH)3
B.2NaHCO3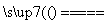 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4NH3+5O2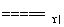 4NO+6H2O
4NO+6H2O
D.Zn+H2SO4===ZnSO4+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列氧化 还原反应中,1 mol H2O得到1 mol电子的是
还原反应中,1 mol H2O得到1 mol电子的是
A.Cl2+H2O===HCl+HClO
B.2Na2O2+2H2O===4NaOH+O2↑
C.2Na+2H2O===2NaOH+H2↑
D.3NO2+H2O===2HNO3+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
某强酸性反应体系中,反应物和生成物共六种物质:PbO2、PbSO4(难溶盐)、Pb(MnO4)2(强电解质)、H2O、X(水溶液呈无色)、H2SO4,已知X是一种盐,且0.1 mol X在该反应中失去3.01×1023个电子。
(1)写出该反应的化学方程式:________________________________________________;
(2)若有9.8 g H2SO4参加反应,则转移电子的物质的量为________;
(3)本反应体系中,若用浓盐酸代替硫酸,用离子方程式表示后果:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列符合“化学反应的绿色化”的是( )
A.实验室制O2:2KClO3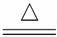 2KCl+3O2↑
2KCl+3O2↑
B.2C2H5OH+O2 2CH3CHO+2H2O
2CH3CHO+2H2O
C.2M+N2P+2Q,2P+M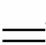 Q(M、N为原料,Q为期望产品)
Q(M、N为原料,Q为期望产品)
D.用铁屑、CuO、稀硫酸为原料制铜:CuO+H2SO4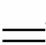 CuSO4+H2O,Fe+CuSO4
CuSO4+H2O,Fe+CuSO4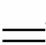 FeSO4+Cu
FeSO4+Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.某醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b
B.在滴有酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7
C.1.0×10-3 mol/L盐酸的pH=3.0,1.0×10-8 mol/L盐酸的pH=8.0
D.若1 mL pH=1的盐酸与100 mL NaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com