
【题目】如图甲是一种利用微生物将废水中的尿素(K2NCONH2)的化学能直接转化为电能,并生成对环境无害物质的装罝;同时利用此装置的电能在铁上镀铜,下列说法中正确的是

A. H+透过质子交换膜由右向左移动
B. 铜电极应与X相连接
C. M电极反应式:H2NCONH2+H2O-6e-== CO2↑+N2↑+6H+
D. 当N电极消耗0.25 mol气体时,铁电极增重16 g
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:
【题目】亚硝酸钙是一种阻锈剂,可用于染料工业,某兴趣小组拟制备Ca(NO2)2并对其性质进行探究。
【背景素材】
I.Ca(NO2)2能被酸性KMnO4溶液氧化成NO3,MnO4-被还原为Mn2+。
II.在酸性条件下,Ca(NO2)2能将I-氧化为I2,S2O32能将I2还原为I。
III.HNO2是具有氧化性的一元弱酸且AgNO2是一种难溶于水的白色化合物。
(1)兴趣小组同学拟利用铜片和某浓度的硝酸制备物质的量之比为1:1的NO和NO2的混合气体,请写出此反应的离子方程式___________________________;
(2)兴趣小组同学拟利用(1)产生的氮氧化物制备Ca(NO2)2,装置如图。

①装置A中导管末端接一玻璃球的作用是___________________________;
②装置B的作用是________________;
③若现有m mol NO2和n mol NO组成的混合气体进入装置C进行尾气处理,欲用a mol/L NaOH溶液吸收,至少需要a mol/L NaOH溶液的体积为____________升;
(3)兴趣小组同学拟测定Ca(NO2)2的纯度(杂质不参加反应),可供选择的试剂:
A.KI(酸性)溶液 B.淀粉溶液
C.Na2S2O3溶液 D.酸性KMnO4溶液
①利用Ca(NO2)2的还原性来测定其纯度,可选择的试剂是____________ (填字母);
②利用Ca(NO2)2的氧化性来测定其纯度,可选择的试剂是____________ (填字母);
(4)兴趣小组同学认为制备的Ca(NO2)2会混有Ca(NO3)2,能用来鉴别二者的试剂(_____)
A.测溶液的PH值 B.加硫酸铁(酸性)溶液
C.加硝酸银溶液 D.加淀粉碘化钾(酸性)溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铵是化工、染织、医药、皮革等工业原料。某硫酸工厂利用副产品Y处理尾气SO2得到CaSO4,再与相邻的合成氨工厂联合制备(NH4)2SO4,工艺流程如下:
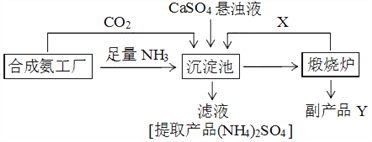
请回答以下问题:
(1)下列有关(NH4)2SO4溶液的说法正确的是_____
A.电离方程式:(NH4)2SO4![]() 2NH4++SO42-
2NH4++SO42-
B.水解离子方程式:NH4++H2O![]() NH3H2O+H+
NH3H2O+H+
C.离子浓度关系:c(NH4+)+c(H+)=c(SO42-)+c(OH–)
D.微粒浓度大小:c(NH4+)>c(SO42-)>c(H+)>c(NH3H2O)>c(OH–)
(2)硫酸工业中,V2O5作催化剂时发生反应2SO2+ O2 ![]() 2SO3,SO2的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择下表中最合适的温度和压强分别是__________。该反应420℃时的平衡常数_____520℃时的平衡常数(填“>”、“<”或“=”)。
2SO3,SO2的转化率与温度、压强有关,请根据下表信息,结合工业生产实际,选择下表中最合适的温度和压强分别是__________。该反应420℃时的平衡常数_____520℃时的平衡常数(填“>”、“<”或“=”)。
| 1.01×105Pa | 5.05×105Pa | 1.01×106Pa |
420℃ | 0.9961 | 0.9972 | 0.9984 |
520℃ | 0.9675 | 0.9767 | 0.9852 |
620℃ | 0.8520 | 0.8897 | 0.9276 |
(3)在2L密闭容器中模拟接触法制备三氧化硫时,若第12分钟恰好达到平衡,测得生成SO3的物质的量为1.2mol,计算前12分钟用氧气表示反应速率v(O2)为___________。
(4)副产品Y是__。沉淀池中发生的主要反应方程式是___________________。
(5)从绿色化学和资源综合利用的角度说明上述流程的主要优点是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验题:
(1)下列说法正确的是_________

A.图1为实验室制备硝基苯的装置
B.图2可以用于测定乙醇分子结构
C.图3装置可以达到验证酸性:CH3COOH > H2CO3 > C6H5OH的目的
D.图4装置可以达到验证溴乙烷发生消去反应生成烯烃的目的
(2)用氧化还原滴定法测定制备得到的TiO2试样中的TiO2的质量分数:在一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作为指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
①TiCl4水解生成TiO2·xH2O的化学方程式为____________________。
②滴定终点的现象是___________________。
③滴定分析时,称取TiO2试样0.2 g,消耗0.1 mol·L—1NH4Fe(SO4)2标准溶液20mL,则TiO2的质量分数为________________。
④若在滴定终点读取滴定管刻度时,俯视标准溶液的液面,使其测定结果__________(填“偏大”“偏小”或“无影响”)。
⑤工业上由H4TiO4可制得钛白粉TiO2。TiO2直接电解还原法生产钛是一种较先进的方法,电解质为熔融的CaCl2,原理如图所示,阴极的电极反应为_________。

(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与Cr![]() 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)为______mol·L-1,此时溶液中c(Cr
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5 mol·L-1)时,溶液中c(Ag+)为______mol·L-1,此时溶液中c(Cr![]() )等于_______mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)
)等于_______mol·L-1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体说法的正确组合是

①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如上图所示)每个Ti4+和12个O2-紧邻
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A.①②③⑥ B.①②④
C.③⑤⑦ D.③⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、N、E、G均是原子序数小于36的元素,XZ2是引起温室效应的主要气体,Z、M同主族且M最外层电子数是电子层数的2倍。Y元素的基态原子最外层有3个未成对电子,次外层有2个电子。N2+核外3d有9个电子,E和 G在周期表中既处于同一周期也处于同一族,且原子序数E比G小2。请回答下列问题:(所有化学式均以元素符号表示)
(1)写出G的外围电子排布式________,X、Y、Z的电负性最大的为___________
(2)XZ32—中中心原子杂化方式为_____________。
(3)比较Z的氢化物(H2Z)和M的氢化物(H2M)的稳定性强弱,并解释其原因是____________。
(4)N与Y可形成的一种具有良好的电学和光学性能的化合物,其晶胞结构如右图所示,则该化合物的化学式为__________。

(5)根据其能量变化示意图,请写出YZ和XZ2反应的热化学方程式 ______________。

(6)检验二价E离子可采用的方法为:在含有这种离子的溶液中加入某种试剂,出现特征蓝色沉淀,其对应的离子方程式是______________。且E在一定条件下可形成体心立方堆积的晶体,设E原子半径为r,请用含r的代数式表示该晶体空间利用率_______________.(不必化简)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:

已知:
i. ![]()
ii. 
iii. 
(以上R、R、R''代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是____________。
(2)B所含官能团的名称是____________。
(3)由C生成D的化学方程式是_______________________________________。
(4)由G生成H的反应是_______反应,1mol F与足量NaOH溶液反应,消耗_______molNaOH。
(5)与 互为同分异构体,且符合下列条件的有机物有_________种。
互为同分异构体,且符合下列条件的有机物有_________种。
①与 含有相同的官能团
含有相同的官能团
②酸性条件下的水解产物能使FeCl3溶液显紫色
③苯环上只有两个取代基
(6)以乙烯为起始原料,结合己知信息选用必要的无机试剂合成CH3CH=CHCH3,写出合成路线______(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下图装置的叙述中,正确的是

A. 若X为铁棒, Y为NaCl溶液, 开关K置于M处, 可减缓铁的腐蚀, 这种方法称为外接电源的阴极保护法
B. 若整个装置为电解精炼铜的装置,则X为粗铜,Y为硫酸铜溶液,开关K置于N处。且电解过程中硫酸铜溶液浓度不变
C. 若X为碳棒, Y为氯化铜溶液, 开关K置于N处, 当产生11.2L气体时,右侧碳棒质量增加6.4g
D. 若X为碳棒, Y为氯化钠溶液, 开关K置于N处, 当电路中有0.01mol电子流过时,假设此时该溶液为100mL,则常温下其pH为13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学组装了如图所示的电化学装置,则下列说法正确的是( )

A.图中甲池为原电池装置,Cu电极发生还原反应
B.实验过程中,甲池左侧烧杯中NO3﹣的浓度不变
C.若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液可能是AgNO3溶液
D.若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量会减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com