
【题目】对称变换是一种建模方法。依据甲烷的一氯代物只有一种,采用如下代换;

下列说法错误的是
A.a、b、c互为同系物B.X的通式一定为CnH2n+2
C.b的同分异构体只有2种(不含立体异构)D.c的三氯代物只有7种(不含立体异构)
【答案】D
【解析】
A.根据烷烃的定义,a、b、c分别为碳原子数为1、5、17的烷烃,它们互为同系物,故A说法正确;
B.X为烷烃,通式为CnH2n+2,故B说法正确;
C.b的同分异构体是CH3CH2CH2CH2CH3、(CH3)2CHCH2CH3,故C说法正确;
D.c中所有甲基都是一样,三个氯原子在同一个-C(CH3)3中甲基上有1种,二个氯原子在一个-C(CH3)中的一个甲基上,另一个氯原子进行移动,有2种结构,二个氯原子分别在一个-C(CH3)3中2个甲基上,另一氯原子进行移动,有2种,三个氯原子分别在三个-C(CH3)3中甲基上取代,有1种结构,共有6种,故D说法错误;
答案:D。


科目:高中化学 来源: 题型:
【题目】一定条件下合成乙烯:6H2(g)+2CO2(g) ![]() CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是 ( )
CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法正确的是 ( )
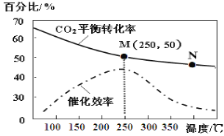
A.M点的正反应速率V正大于N点的逆反应速率V逆
B.若投料比n(H2):n(CO2)=4:1,则图中M点乙烯的体积分数约为5.88%
C.250℃,催化剂对CO2转化率影响最大
D.当温度高于250℃,升高温度,平衡逆向移动导致催化剂的催化效率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的试剂,氢气和二氧化碳在一定条件下可合成甲醇:CO2(g)+3H2 (g) ![]() CH3 OH(g)+H2O(g),在密闭容器中充入3mol氢气和1mol二氧化碳,测得混合气体中甲醇的体积分数与温度的关系如图A所示:
CH3 OH(g)+H2O(g),在密闭容器中充入3mol氢气和1mol二氧化碳,测得混合气体中甲醇的体积分数与温度的关系如图A所示:
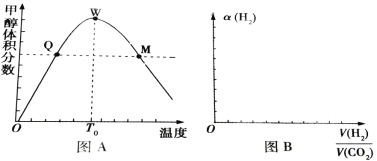
试回答下列问题:
(1)该反应是______(填“放热”或“吸热”)反应。该反应平衡常数的表达式是:______,为了降低合成甲醇的成本可采用的措施是______(任意写一条合理的建议)
(2)解释0~T0内,甲醇的体积分数变化趋势:______。
(3)氢气在Q点的转化率______(填“大于”、“小于”或“等于”,下同)氢气在W点的转化率______;其它条件相同,甲醇在Q点的正反应速率______甲醇在M点的正反应速率。
(4)图B表示氢气转化率α(H2)与投料比![]() 的关系,请在图B中画出两条变化曲线并标出曲线对应的条件,两条曲线对应的条件分别为:一条曲线对应的压强是1.01×105Pa;另一条曲线对应的压强是3.03×105Pa(其它条件相同)
的关系,请在图B中画出两条变化曲线并标出曲线对应的条件,两条曲线对应的条件分别为:一条曲线对应的压强是1.01×105Pa;另一条曲线对应的压强是3.03×105Pa(其它条件相同)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A.用稀盐酸除铁锈:Fe2O3+6H+=2Fe3++3H2O
B.Cl2通入水中:Cl2+H2OH++Cl-+HClO
C.铜与浓硝酸反应生成红棕色气体:3Cu+8H++2NO3-=3Cu2++2NO2↑+4H2O
D.实验室用MnO2和浓盐酸制Cl2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和滴定的误差要求小于0.1%,若用20.00 mL0.2000mol·L-1盐酸滴定20mL0.2000mol·L-1NaOH溶液,则中和滴定曲线中发生突变时的pH范围是(lg2=0.3)( )
A. 4.3~9.7B. 3.7~10.3C. 4.0~10.0D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.乳酸薄荷醇酯( ![]() )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
B.煮熟的鸡蛋不能孵化成小鸡原因是蛋白质变性
C.检验某溶液中是否含有乙醛:在盛有2 mL 10%CuSO4溶液的试管中滴加0.5mL10%NaOH溶液,混合均匀,滴入待检液,加热,看是否产生砖红色沉淀
D.为加快漂白精的漂白速率,使用时可加少量的食盐水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钒(V)及其化合物有着广泛的用途。请回答下列问题:
(1)钒在溶液中的主要聚合状态与溶液的pH关系如图1所示。V2O74-中V元素的化合价是________,溶液中VO3-转化为V2O74-的离子方程式为________。
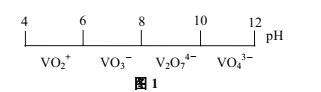
(2)偏钒酸铵是最普通的钒酸盐,将V2O5溶于碳酸钠溶液中(有气体生成),然后加入氯化铵,便可析出偏钒酸铵(NH4VO3),该过程总反应的化学方程式为________;当pH超过8.0时偏钒酸铵会发生转化,其原因是溶液中的VO3-转化为V2O74-、________(请另写出一点原因)。
(3)NH4VO3在高温下分解产生的V2O5可作为硫酸工业中2SO2(g)+O2(g)![]() 2SO3(g)ΔH=pkJ/mol反应的催化剂,其催化原理如图2所示。
2SO3(g)ΔH=pkJ/mol反应的催化剂,其催化原理如图2所示。
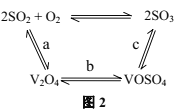
①过程a和过程b的热化学方程式为
V2O5(s)+SO2(g)=V2O4(s)+SO3(g) ΔH=qkJ/mol
V2O4(s)+O2(g)+2SO2(g)=2VOSO4(s) ΔH=rkJ/mol
则过程c的热化学方程式为_________。
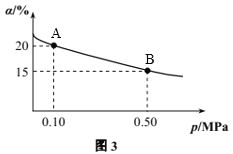
②T℃时反应2SO3(g)![]() 2SO2(g)+O2(g) ΔH>0中SO3的转化率(α)与体系总压强(p)的关系如图3所示。T℃时,将2molSO3置于10L密闭容器中,反应达到平衡后,体系总压强为0.10MPa。则T℃时B点的化学平衡常数Kc=_________。
2SO2(g)+O2(g) ΔH>0中SO3的转化率(α)与体系总压强(p)的关系如图3所示。T℃时,将2molSO3置于10L密闭容器中,反应达到平衡后,体系总压强为0.10MPa。则T℃时B点的化学平衡常数Kc=_________。
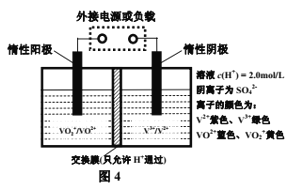
(4)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图4所示。
①充电过程中,右槽溶液颜色逐渐由________色变为________色;
②充电时若转移的电子数为NA个,则左槽溶液中n(H+)的变化量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青出于蓝而胜于蓝,“青”指的是靛蓝,是人类使用历史悠久的染料之一,下列为传统制备靛蓝的过程:
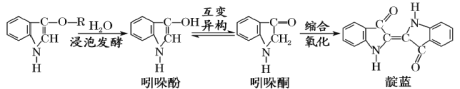
下列说法不正确的是
A.靛蓝的分子式为C16H10N2O2B.浸泡发酵过程发生的反应为取代反应
C.1mol 吲哚酚与H2加成时可消耗4mol H2D.吲哚酚的苯环上的二氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温条件下,用0.100 mol/L的NaOH溶液分别滴定酸HX、HY、HZ,三种酸的体积均为20.00 mL,浓度均为0.100 mol/L,滴定曲线如图所示。下列叙述正确的是

A.酸性强弱:HX>HY>HZ
B.P点对应的溶液中:c(Y-)>c(Na+)>c(HY)>c(H+)>c(OH-)
C.各溶液在滴定过程中任何时刻,溶液中水的电离一直受抑制
D.HZ的电离方程式为:HZ![]() H++Z-
H++Z-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com