
 4NO+6H2O(条件不对或没配平均不给分)(2分)
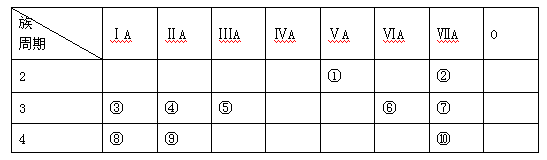
4NO+6H2O(条件不对或没配平均不给分)(2分) 4NO+6H2O。(4)③为Na,④为Mg,Na的化学性质比Mg活泼;可用等量的金属分别于冷水反应,比较二者反应的剧烈程度即可得出结论。
4NO+6H2O。(4)③为Na,④为Mg,Na的化学性质比Mg活泼;可用等量的金属分别于冷水反应,比较二者反应的剧烈程度即可得出结论。

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题
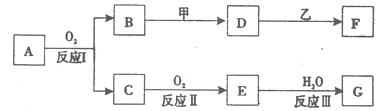
 ;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.M层 | B.N 层 | C.O层 | D.P层 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素代号 | W | R | X | Y | Z | Q | M |
| 原子半径/nm | 0.037 | 0.186 | 0.074 | 0.075 | 0.077 | 0.150 | 0.160 |
| 主要化合价 | +1 | +1 | -2 | -3、+5 | +2、+4 | +3 | +2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 )在一定条件下,2 L的H气体与0.5 L的G气体相混合,若该混合气体被NaOH溶液恰好完全吸收,只生成一种盐。请写出该反应过程中总的化学反应方程式: 。
)在一定条件下,2 L的H气体与0.5 L的G气体相混合,若该混合气体被NaOH溶液恰好完全吸收,只生成一种盐。请写出该反应过程中总的化学反应方程式: 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A | | | |
| | | B | C |

 方程式: 。
方程式: 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com