

分析 (1)Cu是29号元素,其原子核外有29个电子,Cu原子失去一个4s电子、一个3d电子生成二价铜离子,根据构造原理书写二价铜离子的电子排布式;原子轨道中电子处于半满、全满、全空时最稳定;
(2)Cu(g)~Cu+(g),亚铜离子结合水放热582KJ,Cu(g)~Cu+(g)~Cu2+(g),铜离子结合水分子放热2121KJ,亚铜离子变化为铜离子,结合水分子放出热量多于亚铜离子直接结合水分子放出热量多;
(3)铜与类卤素(SCN)2反应生成Cu(SCN)2,SCN分子中硫原子形成两个共用电子对、C原子形成四个共用电子对、N原子形成三个共用电子对,(SCN)2结构式为N≡C-S-S-C≡N,每个分子中含有4个π键,能形成分子间氢键的物质熔沸点较高;
(4)硼元素具有缺电子性,其化合物可与具有孤电子对的分子或离子形成配合物,如BF3能与NH3反应生成BF3•NH3.在BF3•NH3中B原子价层电子对个数是4,根据价层电子对互斥理论确定B原子的杂化方式;
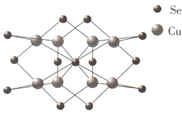
(5)铜和硒可形成的半导体团簇分子,依据分子球棍模型计算所含铜和硒原子数,写出分子式;
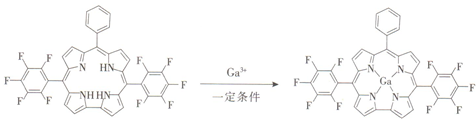
(6)镓与某有机物形成的配合物过程中生成的产物中镓原子和氮原子间形成配位键,由氮原子单方面提供电子对,和镓原子间形成四个配位键;
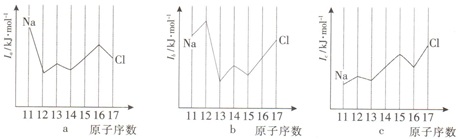
(7)在第三周期元素中,钠失去1个电子后,就已经达到稳定结构,所以钠的第二电离能最大,镁最外层为2个电子,失去2个电子后为稳定结构,所以镁的第二电离能较小,铝最外层有3个电子,失去2个电子后还未达稳定结构,而铝的金属性比镁弱,所以第二电离能比镁略高,硅最外层上2p层有2个电子,失去后,留下2s轨道上有2个电子,相对较稳定,所以硅的第二电离能比铝要低,磷、硫非金属性逐渐增大,第二电离能也增大,由于硫失去一个电子后,3p轨道上是3个电子,是较稳定结构,所以硫的第二电离能要高于氯.
解答 解:(1)Cu是29号元素,其原子核外有29个电子,Cu原子失去一个4s电子、一个3d电子生成二价铜离子,根据构造原理书写二价铜离子的电子排布式为1s22s22p63s23p63d9;原子轨道中电子处于半满、全满、全空时最稳定,二价铜离子价电子排布式为3d9、亚铜离子价电子排布式为3d10,亚铜离子核外电子处于稳定的全充满状态,所以较稳定,
故答案为:1s22s22p63s23p63d9;
(2)Cu(g)~Cu+(g),铜的第一第一电离能为745.5kJ/mol,亚铜离子结合水放热582KJ,Cu(g)~Cu+(g)~Cu2+(g),铜离子结合水分子放热2121KJ,由电离能、Cu+和 Cu2+ 与水结合放出的热量数据可知,Cu+(g)转化Cu2+ (g)再与水结合比Cu+(g)直接水合放出的热量更多,因而在溶液中Cu2+更稳定,
故答案为:由电离能、Cu+和 Cu2+ 与水结合放出的热量数据可知,Cu+(g)转化Cu2+ (g)再与水结合比Cu+(g)直接水合放出的热量更多,因而在溶液中Cu2+更稳定;
(3)铜与类卤素(SCN)2反应生成Cu(SCN)2,SCN分子中硫原子形成两个共用电子对、C原子形成四个共用电子对、N原子形成三个共用电子对,(SCN)2结构式为N≡C-S-S-C≡N,每个分子中含有4个π键,则1mol(SCN)2中含有π键的数目为4NA;
能形成分子间氢键的物质熔沸点较高,异硫氰酸分子间可形成氢键,而硫氰酸不能形成分子间氢键,所以异硫氰酸熔沸点高于硫氰酸,
故答案为:4NA;异硫氰酸分子间可形成氢键,而硫氰酸不能;
(4)硼元素具有缺电子性,其化合物可与具有孤电子对的分子或离子形成配合物,如BF3能与NH3反应生成BF3•NH3.在BF3•NH3中B原子价层电子对个数是4,根据价层电子对互斥理论确定B原子的杂化方式为sp3,
故答案为:sp3;
(5)分子的球棍模型中含铜原子8个含硒原子13个,则分子式为Cu8Se13,
故答案为:Cu8Se13;
(6)镓原子和氮原子间形成配位键,由氮原子单方面提供电子对,和镓原子间形成四个配位键,画出的配位键图示为: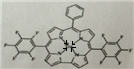
故答案为: ;
;
(7)在第三周期元素中,钠失去1个电子后,就已经达到稳定结构,所以钠的第二电离能最大,镁最外层为2个电子,失去2个电子后为稳定结构,所以镁的第二电离能较小,铝最外层有3个电子,失去2个电子后还未达稳定结构,而铝的金属性比镁弱,所以第二电离能比镁略高,硅最外层上2p层有2个电子,失去后,留下2s轨道上有2个电子,相对较稳定,所以硅的第二电离能比铝要低,磷、硫非金属性逐渐增大,第二电离能也增大,由于硫失去一个电子后,3p轨道上是3个电子,是较稳定结构,所以硫的第二电离能要高于氯,a为第二电离能为I2、b为第三电离能为I3、c为第一电离能为I1,选B,
故答案为:B.
点评 本题考查物质结构和性质,为高频考点,侧重考查学生空间想象能力及计算能力,涉及配位键形成、原子杂化方式判断、原子核外电子排布等知识点,主要是图象分析和数据分析、电离能的理解应用,题目难度较大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | v(H2)=v(N2)=v(NH3) | B. | v(H2)=3 v(N2) | C. | v(N2)=2 v(NH3) | D. | 2v(NH3)=3v(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| a | |||
| b | c | d |
| A. | 离子半径:b>c>d>a | |
| B. | bn+与dm-在水溶液中可形成化合物bmdn | |
| C. | 简单氢化物的稳定性:a<c | |
| D. | b和d的最高价氧化物对应的水化物可相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在溶液中加酸化的BaCl2溶液,溶液出现白色沉淀,证明原溶液中有SO42- | |
| B. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 | |
| C. | 气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气 | |
| D. | 将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气 | |
| B. | 检测时,电解质溶液中的H+向负极移动 | |
| C. | 正极上发生的反应为O2+4e-+2H2O═4OH- | |
| D. | 电池反应的化学方程式为CH3CH2OH+O2═CH3COOH+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com