
| A. | C3H6 | B. | C2H4 | C. | C4H6 | D. | C2H2 |
分析 1体积气态烃A最多能和2体积HCl加成生成氯代烃,说明烃中含有2个C=C或1个C≡C,此氯代烃lmol能和8molCl2发生取代反应,说明氯代烃中含有8个H原子,其中有2个H原子为加成反应得到,则烃A分子中应含有6个H原子,以此进行判断.
解答 解:1体积气态烃A最多能和2体积HCl加成生成氯代烃,说明烃中含有2个C=C或1个C≡C,此氯代烃lmol能和8molCl2发生取代反应,说明氯代烃中含有8个H原子,其中有2个H原子为加成反应得到,则烃A分子中应含有6个H原子,选项中只有C4H6符合,
故选C.
点评 本题考查有机物分子式的确定,为高频考点,题目有利于培养学生的计算能力和分析能力,难度不大,侧重考查加成反应与取代反应,注意理解有机物的加成和取代反应特征.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{576v}$mol/L | B. | $\frac{125a}{36v}$mol/L | C. | $\frac{250a}{36v}$mol/L | D. | $\frac{250a}{48v}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
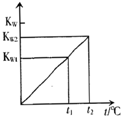 水的离子积常数KW与温度t(℃)的关系如图所示:
水的离子积常数KW与温度t(℃)的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
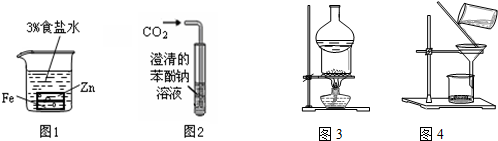
| A. | 图1中正极反应是Zn-2e-=Zn2+ | |
| B. | 图2可用于比较碳酸、苯酚酸性的强弱 | |
| C. | 图3可用于I2与NH4Cl混合物的分离 | |
| D. | 图4用于去除Fe(OH)3胶体中含有的可溶性物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向H2S水溶液中加入NaOH有利于S2-增多 | |
| B. | 鼓入过量空气有利于SO2转化为SO3 | |
| C. | 高压对合成氨有利 | |
| D. | 500℃左右比室温更有利于合成氨的反应 (合成氨反应是放热反应) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在组装蒸馏装置时,温度计的水银球应伸入液面下 | |
| B. | 用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏 | |
| C. | 在苯甲酸重结晶实验中,在冷却结晶过程中温度越低越好 | |
| D. | 在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后,要冷却到常温才过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
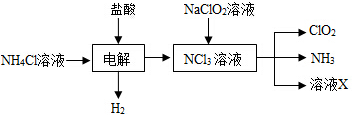
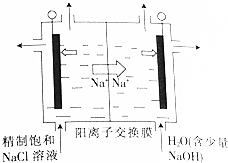
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表是元素按原子序数大小排列而成的 | |
| B. | 元素原子的电子层数等于其所在周期的周期序数 | |
| C. | 元素原子的最外层电子数等于其所在族的族序数 | |
| D. | 元素周期表中共有18列,16个族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com