
| A. | 28g${\;}_{6}^{14}$C中含有的质子数为14NA | |
| B. | 1mol苯乙酸中所含碳碳双键数为4NA | |
| C. | 1L 2mol/L的NaClO水溶液中含有的氧原子数为2NA | |
| D. | 标准状况下,3.36L NO2和足量水充分反应转移的电子数为0.1NA |
分析 A.结合n=$\frac{m}{M}$及质子数为6计算;
B.苯乙酸中不含碳碳双键;
C.水中含O原子;
D.n(NO2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,发生3NO2+H2O=2HNO3+NO,该反应转移2e-,以此来解答.
解答 解:A.n=$\frac{m}{M}$=$\frac{28g}{14g/mol}$=2mol,含质子数为2mol×6×NA=12NA,故A错误;
B.苯乙酸中不含碳碳双键,则不能计算碳碳双键数目,故B错误;
C.水中含O原子,则溶液中含有的氧原子数远大于2NA,故C错误;
D.n(NO2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,发生3NO2+H2O=2HNO3+NO,该反应转移2e-,则和足量水充分反应转移的电子数为0.15mol×$\frac{1}{3}$×(4-2)×NA=0.1NA,故D正确;
故选D.
点评 本题考查物质的量计算及阿伏伽德罗常数,为高频考点,把握物质的量的相关计算公式、物质的组成、氧化还原反应等为解答的关键,侧重分析与计算能力的考查,题目难度不大.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:解答题
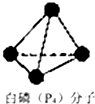 氨是重要的化工原料,用途广泛.
氨是重要的化工原料,用途广泛.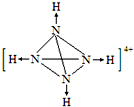 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去):
已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去): ;D
;D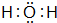 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.4g | B. | 6g | C. | 12.4g | D. | 8.8g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | n(Cl2)、n(HClO)和n(ClO-)之和不随pH变化而变化 | |
| B. | 当pH逐渐增大时,HClO先增大后减小 | |
| C. | 当pH>8.5时,c(H+)=c(OH-)+c(ClO-)+c(Cl-) | |
| D. | K1、K2均是通过曲线交点计算得出的酸的电离平衡常数 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:填空题
汽车常装有安全气囊,当发生强烈碰撞时,瞬间引发以下反应:2NaN3=2Na+3N2↑,所产生的气体快速充满气囊,可以达到保护车内人员的目的.
(1)若气囊中装有130g NaN3,则其物质的量是_______________.
(2)若130g NaN3完全分解,在标准状况下,气囊膨胀的体积约为_______________.
(3)该反应中的氧化剂是 氧化产物是__________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
224mL某气体在标准状况下的质量为0.32g,该气体的摩尔质量为
A.32g•mol﹣1 B.64 C.64g•mol﹣1 D.64g
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com