
分子式为C5H10O3的有机物与NaHCO3溶液反应时,生成C5H9O3Na;而与金属钠反应时生成C5H8O3Na2。则该有机物的同分异构体的种类(不考虑立体异构)有
A.10种 B.11种 C.12种 D.13种
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
在一定体积的密闭容器中,进行如下的化学反应CO2(g)+H2(g)  CO(g)+H2O(g),其
CO(g)+H2O(g),其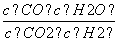 =K,K被称为化学平衡常数,其中K和温度的关系如下表:
=K,K被称为化学平衡常数,其中K和温度的关系如下表:
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1. 0 | 1.7 | 2.6 |
根据以上信息推断以下说法正确的是( )
A.此反应为放热反应
B.此反应只有达到平衡时,密闭容器中的压强才不会变化
C.此反应达到1000 ℃时的反应速率比700 ℃时大
D.该反应的化学平衡常数越大,反应物的转化率越低
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,下列说法正确的是双选) )。
A.pH=12的NaOH溶液中,cH+)=10-12 mol·L-1,将溶液稀释为原体积的10倍后cH+)=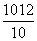 mol·L-1=10-13mol·L-1
mol·L-1=10-13mol·L-1
B.pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后,因生成的CH3COONa
水解,所以由水电离出的cH+)<10-7mol·L-1
C.pH=2的盐酸、pH=2的醋酸中由水电离出的cH+)均为10-12 mol·L-1
D.pH=11和pH=13的NaOH溶液等体积混合后,溶液中的cH+)=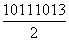 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在三个体积均为1.0 L 的恒容密闭容器中发生反应:
2CH3OHg)CH3OCH3g)+H2Og)
| 容器 编号 | 温度℃) | 起始物质的量mol) | 平衡物质的量mol) | |
| CH3OHg) | CH3OCH3g) | H2Og) | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
下列说法正确的是双选) )。
A.该反应的正反应为放热反应
B.达到平衡时,容器Ⅰ中的CH3OH体积分数比容器Ⅱ中的小
C.容器Ⅰ中反应达到平衡所需时间比容器Ⅲ中的长
D.若起始时向容器Ⅰ中充入CH3OH 0.15 mol、CH3OCH3 0.15 mol和H2O 0.10 mol,则反应将向正反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
“心得安”是治疗心脏病的药物,下面是它的一种合成路线(具体反应条件和部分试剂略):
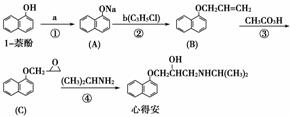
回答下列问题:
(1)试剂a是________,试剂b的结构简式为________,b中官能团的名称是________。
(2)③的反应类型是________。
(3)心得安的分子式为________。
(4)试剂b可由丙烷经三步反应合成:
C3H8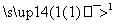 X
X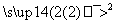 Y
Y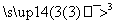 试剂b
试剂b
反应1的试剂与条件为________,反应2的化学方程式为______________, 反应3的反应类型是________。
(5)芳香化合物D是1萘酚的同分异构体,其分子中有两个官能团,能发生银镜反应,D能被 KMnO4酸性溶液氧化成E(C2H4O2)和芳香化合物F(C8H6O4),E和F与碳酸氢钠溶液反应均能放出CO2气体,F芳环上的一硝化产物只有一种。D的结构简式为________;由F生成一硝化产物的化学方程式为________________,该产物的名称是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氮氧化物能造成光化学烟雾,引起大气污染,用以下方法可以消除。
Ⅰ.活性炭还原法处理氮氧化物。若向2L密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应生成甲和乙,甲和乙均为参与大气循环的物质,反应进行到不同时间测得各物质的物质的量浓度如下:
|
| NO | 甲 | 乙 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
| 40 | 0.032 | 0.034 | 0.017 |
| 50 | 0.032 | 0.034 | 0.017 |
(1)该反应的化学方程式为_____________________________________________
(2)T1℃时,该反应的平衡常数K=______________
(3) 30min时改变的的条件是_______________。若30min后升高温度至T2,达到平衡时,容器中NO、甲、乙的浓度之比为2∶1∶1,则反应的△H__________0(填“<”、“=”、“>”)。
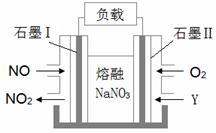 Ⅱ.以NO、O2、熔融NaNO3组成的燃料电池装置如图所示,在使用过程中石墨电极Ⅰ生成NO2。
Ⅱ.以NO、O2、熔融NaNO3组成的燃料电池装置如图所示,在使用过程中石墨电极Ⅰ生成NO2。
(4)石墨电极Ⅰ的反应式为______________________;为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,即必须在石墨电极Ⅱ电极处通入一种氧化物Y,Y是_______________(填物质的化学式)。
Ⅲ.CH4催化还原法。已知:
①CH4(g)+4NO2(g)  4NO(g)+CO2(g)+2H2O(l) △H=-622kJ/mol
4NO(g)+CO2(g)+2H2O(l) △H=-622kJ/mol
②CH4(g)+2NO2(g)  N2(g)+CO2(g)+2H2O(l) △H=-955kJ/mol
N2(g)+CO2(g)+2H2O(l) △H=-955kJ/mol
③H2O(g)=H2O(l) △H=-44.0kJ/mol
(5)写出CH4(g)与NO(g)反应生成N2(g)、CO2(g)和H2O(g)的热化学方程式______________________________________________________________。
(6)假设在某温度下反应①的速率(v1)大于反应②的速率(v2)则下列反应过程能量变化示意图正确的是________(填写正确选项的字母)。
|
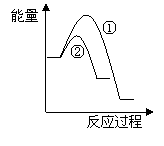
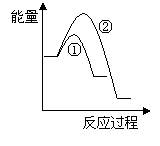
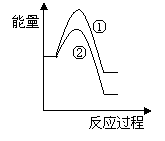
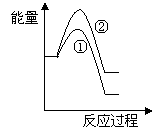


(7)恒温恒容条件下,假设反应①和②同时发生,且v1>v2,请在下图中画出反应体系中c(NO)随时间t变化的总趋势图。
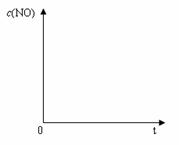
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.在标况下,11.2 L NO与11.2 L O2混合后所含分子数为0.75NA
B.常温常压下,16 g O3所含的电子数为8NA
C.0.1 mol Na2O2晶体中含有0.4NA个离子
D.铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物A~H均含苯环,它们之间的转化关系如下。已知:B与FeCl3溶液混合无颜色变化。
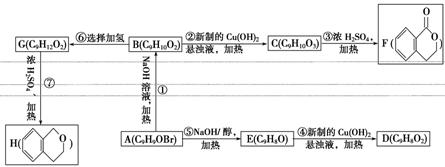
回答下列问题:
(1)B的结构简式为________。
(2)①~⑦中属于取代反应的是________(填序号)。
(3)写出一种可鉴别D、F的试剂:________。
(4)写出反应⑦的化学方程式:______________________________________________。
(5)写出同时符合下列条件的C的同分异构体的结构简式:________________________
________________________________________________。
①化合物是1,3,5三取代苯
②苯环上的三个取代基中分别含有醇羟基、酚羟基和醛基
查看答案和解析>>
科目:高中化学 来源: 题型:
不能用化学平衡移动原理说明的事实是( )
A.合成氨在高压下进行是有利的
B.温度过高对合成氨不利
C.使用催化剂能使合成氨速率加快
D.及时分离从合成塔中出来的混合气,有利于合成氨
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com