
【题目】A、B、C、D均为短周期元素。A、B可形成两种液态化合物甲和乙,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。A、B、D可组成离子化合物,该晶体化学式为B4A3D2,其水溶液呈弱酸性。B与D可形成一种极易溶于水的碱性气体X。B与C可形成极易溶于水的酸性气体Y。已知X分子与乙分子中的电子数相等,Y分子与甲分子中的电子数相等。请回答:
(1)A元素为___,甲的电子式为____________。
(2)常温下,pH为a的Y溶液与pH为b的氢氧化钠溶液按体积比1∶10混合后,正好完全反应,则a与b的关系为______。
(3)已知X在液态时和水一样,可发生微弱的电离,产生两种含相同电子数的粒子,请写出它电离方程式:____________________。
(4)将X和Y的稀溶液按某种比例混合,
①若所得溶液中只含一种溶质,则该溶质是______,溶液中离子浓度的大小顺序为____________________________;
②若该溶液是由体积相等的X和Y溶液混合而成,且恰好呈中性,则混合前c(X)____c(Y),混合前酸中c(H+)和碱中c(OH-)的关系c(H+)____c(OH-)(填“大于”、“等于”、“小于”)。
【答案】氧 ![]() a+b=13 2NH3
a+b=13 2NH3![]() NH4++NH2- NH4Cl c(Cl-)>c(NH4+)>c(H+)>c(OH-) 大于 大于
NH4++NH2- NH4Cl c(Cl-)>c(NH4+)>c(H+)>c(OH-) 大于 大于
【解析】
A、B、C、D均为短周期元素;A、B可形成两种液态化合物甲和乙,其最简式分别为BA和B2A,则A、B分别为O、H,甲为过氧化氢,乙为水;B与D可形成一种极易溶于水的碱性气体X,X分子与乙分子中的电子数相等,则X为氨气,D为N;A、B、D可组成离子化合物,该晶体化学式为B4A3D2,该晶体为硝酸铵;B与C可形成极易溶于水的酸性气体Y,Y分子与过氧化氢分子中的电子数相等,为18,则C为Cl,Y为HCl;
(1)根据分析可知,A为O;甲为过氧化氢,过氧化氢的电子式为:![]() ;
;
(2)常温下,pH为a的HCl溶液与pH为b的氢氧化钠溶液按体积比1∶10混合后,正好完全反应,则氢离子、氢氧根离子的物质的量相等,则10-a![]() V=10b-14
V=10b-14![]() 10V,解得a+b=13;
10V,解得a+b=13;
(3)已知氨气在液态时和水一样,可发生微弱的电离,产生两种含相同电子数的粒子,分别为铵根离子和NH2-离子,电离的方程式为:2NH3![]() NH4++NH2-;
NH4++NH2-;
(4)①氨气与盐酸反应只生成一种溶质,则为氯化铵;氯化铵为强酸弱碱盐,少量的铵根离子发生水解生成一水合氨与氢离子,则溶液中离子浓度由大到小的顺序为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
②由体积相等的氨水和HCl溶液混合而成,且恰好呈中性,则混合后溶液中氢离子与氢氧根离子浓度相等,氯化铵溶液中存在一定量的一水合氨分子,则混合前氨水的浓度大于盐酸的浓度;氨水为弱碱水溶液,盐酸为强酸,则混合前酸中氢离子浓度大于碱中氢氧根离子的浓度。


科目:高中化学 来源: 题型:
【题目】用废铁屑制备磁性胶体粒子,制取过程如下:

下列说法不正确的是
A. 用Na2CO3溶液浸泡是为了除去废铁屑表面的油污
B. 通入N2是防止空气中的O2氧化二价铁元素
C. 加适量的H2O2是为了将部分Fe2+氧化为Fe3+,涉及反应:H2O2+2Fe2++2H+=2Fe3++2 H2O
D. 溶液A中Fe2+和Fe3+的浓度比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有CO、NOx等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
(1)已知 4CO(g)+2NO2(g)![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol1
①该反应在________________(填“高温、低温或任何温度”)下能自发进行。
②对于该反应,改变某一反应条件(温度T1>T2),下列图象正确的是_______(填序号)。
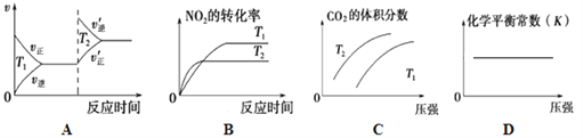
③某实验小组模拟上述净化过程,一定温度下,在2L的恒容密闭容器中,起始时按照甲、乙两种方式进行投料,经过一段时间后达到平衡状态,测得甲中CO的转化率为50%,则该反应的平衡常数为__________;两种方式达平衡时,N2的体积分数:甲______乙( 填“>、=、<或不确定”,下同),NO2的浓度:甲______乙。

(2)柴油汽车尾气中的碳烟(C)和NOx可通过某含钴催化剂催化消除。不同温度下,将模拟尾气(成分如下表所示)以相同的流速通过该催化剂测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图所示。
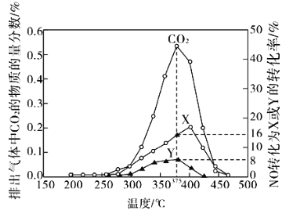
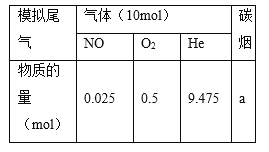
①375℃时,测得排出的气体中含0.45 mol O2和0.0525 mol CO2,则Y的化学式为________。
②实验过程中采用NO模拟NOx,而不采用NO2的原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氧化铝样品中含有氧化铁和二氧化硅(一种酸性氧化物)杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。回答下列问题:
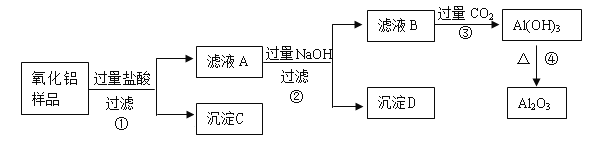
(1)在操作①中要用到的玻璃仪器有_____________________________________________;
(2)沉淀C的化学式是_____________。滤液B中含有的溶质有__________(写化学式);
(3)步骤③的离子方程式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答实验室配制0.1 mol/L的NaOH溶液500 mL实验中的下列问题。
(1)需NaOH_________g。
(2)有以下仪器:
①烧杯 ②100 mL量筒 ③药匙 ④500 mL容量瓶 ⑤胶头滴管 ⑥托盘天平,配制时,还缺少的玻璃仪器是__________________。
(3)下列称量NaOH的操作中,正确的是_______________。(填序号,下同)
①把NaOH直接放在托盘上称量
②把NaOH放在称量纸上称量
③把NaOH放入烧杯中称量
(4)使用容量瓶前必须进行的一步操作是_____________________________。
(5)配制过程中,下列操作会引起误差偏高的是_______________________。
①未洗涤烧杯、玻璃棒
②NaOH溶液未冷却至室温就转移到容量瓶中
③容量瓶不干燥,含有少量蒸馏水
④称量NaOH的时间太长
⑤定容时俯视刻度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中,容器甲内充入0.1 mol NO气体。干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体。恒温下,容器甲中活塞缓慢由D处向左移动,当移至C处时容器体积缩至最小,为原体积9/10,干燥管中物质的质量增加了2.24 g。随着CO2的继续通入,活塞又逐渐向右移动。下列说法中正确的是
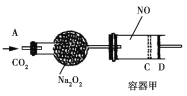
A. 活塞从D处移动到C处的过程中,通入的CO2气体为2.24 L(标准状况)
B. NO2转化为N2O4的转化率为20%
C. 容器甲中NO已反应完
D. 活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至D处,则a小于0.01
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是一系列含硫化合物的转化关系(反应中生成的水已略去),其中说法正确的是
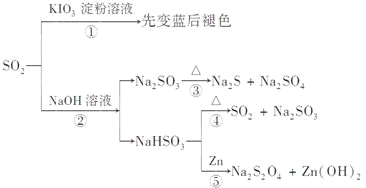
A.反应①说明SO2具有漂白性,反应②说明SO2具有酸性
B.反应②中生成物n(Na2SO3):n(NaHSO3)=1:1时,则反应物n(SO2):n(NaOH)=1:2
C.反应③④⑤均属于氧化还原反应
D.工业上可利用反应②和反应④回收SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究Cl2、SO2同时通入水中所发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
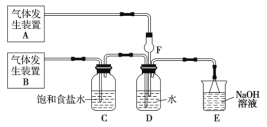
(1)该化学兴趣小组的同学采用Na2SO3与质量分数为70%的硫酸为原料制取SO2,采用MnO2与浓盐酸为原料制取Cl2。在此实验中,仪器![]() 的作用是______;气体发生装置B应选择下列装置中的____________(填序号)。
的作用是______;气体发生装置B应选择下列装置中的____________(填序号)。
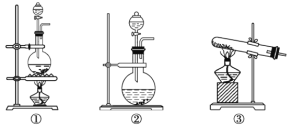
(2)为验证通入D装置中的气体是Cl2过量还是SO2过量,该化学兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④酸性高锰酸钾溶液
若Cl2过量,取适量D中溶液滴加至盛有______(填序号)的试管中,再加入______(填序号),产生的现象是______。
若SO2过量,取适量D中溶液滴加至盛有______(填序号)的试管中,产生的现象是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体化合物A,按图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色。
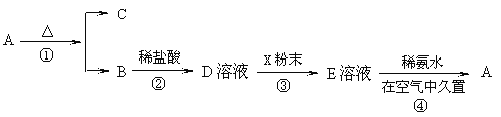
回答下列问题:(1)物质A是___(填化学式)。
(2)反应②的离子反应方程式为___。
(3)反应④的化学反应方程式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com