
| 可以鉴别的物质 | 实验现象 | 有关反应的化学方程式 |
| . |
分析 加入Ba(OH)2溶液,只有Na2SO4和NH4Cl与Ba(OH)2溶液反应,可分别生成沉淀和气体,其它两种物质不反应,以此解答该题.
解答 解:KCl、Na2SO4、NaCl、NH4Cl中取少量上述溶液于4支试管中,然后分别加入Ba(OH)2溶液并加热,Na2SO4和Ba(OH)2溶液反应生成硫酸钡白色沉淀,方程式为Na2SO4+Ba(OH)2=BaSO4↓+2H2O,NH4Cl与氢氧化钡溶液在加热条件下发生2NH4Cl+Ba(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑BaCl2+2H2O,湿润的红色石蕊试纸在试管口检验,试纸变蓝,KCl、NaCl不反应,
故答案为:KCl、NaCl;
| 可以鉴别的物质 | 实验现象 | 有关反应的化学方程式 |
| Na2SO4 | 生成沉淀 | Na2SO4+Ba(OH)2=BaSO4↓+2H2O |
| NH4Cl | 湿润的红色石蕊试纸变蓝 | 2NH4Cl+Ba(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑BaCl2+2H2O |
| . |
点评 本题考查物质的检验和鉴别的实验设计,侧重于学生的分析、实验能力的考查,注意把握物质的性质以及反应现象,学习中注意元素化合物知识的学习和积累,难度不大.


科目:高中化学 来源: 题型:选择题
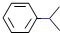
| A. | 异丙苯的分子式为C9H12 | |
| B. | 异丙苯的沸点比苯高 | |
| C. | 异丙苯中碳原子可能都处于同一平面 | |
| D. | 异丙苯和苯为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 共价化合物中一定没有离子键,离子化合物中一定没有共价键 | |
| B. | 金属原子与非金属原子间一定以共价键相结合 | |
| C. | 由不同种原子形成的纯净物一定是化合物 | |
| D. | 石墨转化成全刚石要吸收热量,石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂能够降低化学反应的反应热(△H) | |
| B. | 金属发生吸氧腐蚀时,被腐蚀的速率与氧气浓度无关 | |
| C. | 原电池中发生的反应达平衡时,该电池仍有电流产生 | |
| D. | 在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(NH4+)>c(Cl-)>c(H+)>c(OH-) | B. | c(NH4+)>c(Cl-)>c(OH-)>c(H+) | ||
| C. | c(Cl-)>c(NH4+)>c(H+)>c(OH-) | D. | c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀. |
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com