
 为了验证同浓度同体积的盐酸和醋酸的酸性不同,在同温同压下,设计如下实验:
为了验证同浓度同体积的盐酸和醋酸的酸性不同,在同温同压下,设计如下实验:| 24g×0.1mol/l×0.1L |
| 2mol |
| 0.1mol/L×0.1L×1mol |
| 2mol |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、说明金刚石的内能比石墨低 |
| B、说明红磷比白磷稳定 |
| C、说明红磷比金刚石稳定 |
| D、此种变化为物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4项 | B、5项 | C、6项 | D、7项 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤 | 实验现象 | 解释(用化学方程式表示) | |
| ① | 将充满NO2的倒立在盛有水的水槽中,拨去橡皮塞,轻轻晃动试管. | 试管内气体由 | |
| ② | |||
| ③ | 重复步骤②的操作数次,直至液体充满整个试管. | 试管内充满无色液体. | 总反应方程式: |

查看答案和解析>>
科目:高中化学 来源: 题型:
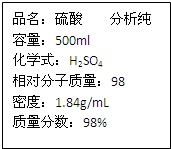 用标签如右图的浓硫酸配置500mL0.5mol?L-1稀硫酸,请回答下列问题:
用标签如右图的浓硫酸配置500mL0.5mol?L-1稀硫酸,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com