
| A. | 2MnO2+2NH4++2e-═2MnO(OH)+2NH3 | B. | Zn-2e-═Zn2+ | ||
| C. | [Zn(NH3)2]2++2e-═Zn+2NH3 | D. | Mn4++e-═Mn3+ |
分析 由电池反应Zn+2MnO2+2NH4Cl(aq)═2MnO(OH)(s)+[Zn(NH3)2]Cl2(aq),Zn失去电子被氧化,Mn得到电子被还原,以此来解答.
解答 解:由电池反应Zn+2MnO2+2NH4Cl(aq)═2MnO(OH)(s)+[Zn(NH3)2]Cl2(aq),Zn失去电子被氧化,Mn得到电子被还原,则负极上Zn失去电子,而正极上Mn得到电子,正极反应为2MnO2+2NH4++2e-═2MnO(OH)+2NH3,
故选A.
点评 本题考查原电池及电极反应,为高频考点,把握电池反应中元素的化合价变化、电极反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应的应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
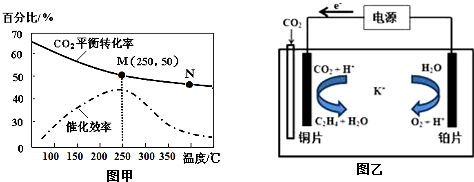
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应大多数是放热反应,分解反应全都是吸热反应 | |
| B. | C(金刚石,s)+O2(g)=CO2(g)的反应热等于1molO2的键能与1molCO2中键能的差 | |
| C. | 热化学方程式中,反应条件可以不写,而且各物质前的化学计量数可以是分数 | |
| D. | 如果反应物所具有的总能量小于生成物所具有的总能量,则发生的反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 依据丁达尔现象可将分散系分为溶液、胶体与浊液 | |
| B. | 用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率 | |
| C. | 制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸 | |
| D. | 在3S+6KOH=2K2S+K2SO3+3H2O反应中,作氧化剂的S原子与作还原剂的S原子的物质的量之比是1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器甲中分子总数多 | B. | 容器甲中C的浓度大 | ||
| C. | 容器甲中反应速率快 | D. | 容器甲中转化率大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②⑤ | C. | ②③⑤ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 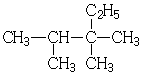 2,3-二甲基-3-乙基丁烷 | B. | 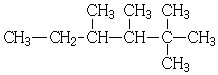 2,2,3,4-四甲基己烷 | ||
| C. |  对二甲苯 | D. |  2,4,4-三甲基戊烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com