
����Ŀ������ʵ�ˮ��Һ�д��ڵ���ƽ�⡣
��1�������dz��������ᡣ
�ٴ�����ˮ��Һ�еĵ��뷽��ʽΪ____________��
�����з����У�����ʹ������Һ��CH3COOH����̶��������_______������ĸ��ţ���
a �μ�����Ũ���� b ����Һ
c ��ˮϡ�� d �������������ƾ���
��2����0.1 mol��L-1 NaOH��Һ�ֱ�ζ������Ϊ20mL��Ũ�Ⱦ�Ϊ0.1 mol��L-1������ʹ�����Һ���õ��ζ���������ҺpH�����NaOH��Һ������仯�������ζ����ߡ�
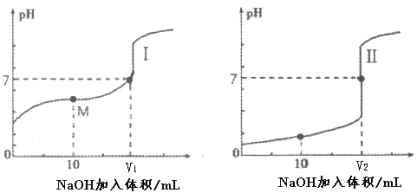
�ٵζ������������___________������I��������������
�ڵζ���ʼǰ��0.1 mol��L-1 NaOH��0.1 mol��L-1�������0.1 mol��L-1����������Һ����ˮ�������c(H+)������_______��Һ��
��ͼI�У�V=10ʱ����Һ�е�c(H+)_________c(OH-) ������>��������������<������ͬ����c(Na+)_________c(CH3COO-)��
��3���±�Ϊijͬѧ����25��ʱ���ס���������Һ��pH��
�� | �� | |
pH | 11 | 11 |
��Һ | ��ˮ | ����������Һ |
�ټ���Һ�е�c(OH-) =___________mol/L��
��25��ʱ��������ļס�������Һ���Ũ�ȵ����ᷴӦ�����ĵ������������_____�ҡ�
�ۼס�����Һ����ˮϡ��10����������Һ��pH����_____�ҡ�
��4��ú̿��ҵ�о������������SO2��Ϊ��ֹ��Ⱦ���������������շ����д������������ʿ���������SO2����____________��
A H2O2 B Na2CO3 C Na2SO3 D Ca(OH)2
��5���±��Ǽ��ֳ�������ĵ��볣��
��ѧʽ | CH3COOH | H2SO3 | HClO | H2CO3 |
���� ���� | 1.8��10-5 | K1=1.23��10-2 K2=6.6��10-8 | 3.0��10-8 | K1=4.4��10-7 K2=4.7��10-11 |
/span>
���·�Ӧ��Ӧ�����ӷ���ʽ��ȷ����___________��
A Na2CO3��Һ��������SO2��CO32-+SO2+H2O = SO32-+HCO3-
B Ư��Һ��Ч��ԭ����ClO-+CO2+H2O = HClO+HCO3-
C ����������Һ��������SO2��ClO-+SO2+H2O = HClO+SO32-
D �����ˮ���е�CaCO3��2CH3COOH+CaCO3 = Ca2++2CH3COO-+H2O+CO2��
���𰸡�CH3COOH![]() CH3COO�� + H+ bc I CH3COOH > < 0.001 > > ABCD ABD
CH3COO�� + H+ bc I CH3COOH > < 0.001 > > ABCD ABD
��������
��1���ٴ��������ᣬ����ȫ���롣
��a. �μ�����Ũ���ᣬ�����������ӵ�Ũ�ȣ�ƽ�����ƣ� CH3COOH����̶ȼ�С��
b. ����Һ���ٽ�������룬CH3COOH����̶�����
c. ��ˮϡ�ͣ��ٽ�������룬CH3COOH����̶�����
d .�������������ƾ��壬�����˴��������Ũ�ȣ�ƽ�����ƣ� CH3COOH����̶ȼ�С��
��2����������ǿ�ᡢ���������ᣬ0.1 mol��L-1��������c(H+)=0.1mol/L��0.1 mol��L-1������c(H+)<0.1mol/L�����������pH=1,�����pH>1��
����������ˮ���룬����c(H+)Խ����c(OH-)Խ��������ˮ�ĵ���̶�Խ��
��ͼI�У�V=10ʱ��pH<7������c(H+)>c(OH-)�����ݵ���غ�c(H+)+c(Na+)=c(OH-)+c(CH3COO-)����c(Na+)<c(CH3COO-)��
��3���ټ���Һ��pH =11��c(H+)=10-11 mol/L��c(OH-) =10-3mol/L��
�����ڰ�ˮ�����c(NH3H2O) >10-3mol/L��c(NaOH) =10-3mol/L��
�����ڰ�ˮ�����ϡ�����е���̶�����n(OH-)����NaOH��ǿ�
��4��A .H2O2 +SO2=H2SO4
B. Na2CO3 +SO2= Na2SO3 + CO2
C. Na2SO3 +SO2+H2O= 2NaHSO3
D Ca(OH)2+SO2= CaSO3��+H2O��
��5�����ݱ����ṩ�����ݺ�ǿ���������ԭ�������ɵá�
��1���ٴ��������ᣬ����ȫ���룬���뷽��ʽΪCH3COOH![]() CH3COO�� + H+���ʴ�Ϊ��CH3COOH
CH3COO�� + H+���ʴ�Ϊ��CH3COOH![]() CH3COO�� + H+��
CH3COO�� + H+��
��a. �μ�����Ũ���ᣬ�����������ӵ�Ũ�ȣ�ƽ�����ƣ� CH3COOH����̶ȼ�С����a��ѡ��
b. ����Һ���ٽ�������룬CH3COOH����̶�����bѡ��
c. ��ˮϡ�ͣ��ٽ�������룬CH3COOH����̶�����cѡ��
d .�������������ƾ��壬�����˴��������Ũ�ȣ�ƽ�����ƣ� CH3COOH����̶ȼ�С����d��ѡ��
��ѡbc��
��2����������ǿ�ᡢ���������ᣬ0.1 mol��L-1��������c(H+)=0.1mol/L��0.1 mol��L-1������c(H+)<0.1mol/L�����������pH=1,�����pH>1������ͼ֪��I�Ǵ������ߣ������������ߣ��ʴ�Ϊ��I��
����������ˮ���룬����c(H+)Խ����c(OH-)Խ��������ˮ�ĵ���̶�Խ��������c(H+)��������������Һ��c(OH-)�����ڴ�����c(H+)����������ˮ����̶�:����=��������>���ᣬ��ζ���ʼǰ��������Һ����ˮ�������c(H+)������0.1 mol��L-1���ᣬ�ʴ�Ϊ�����ᡣ
��ͼI�У�V=10ʱ��pH<7������c(H+)>c(OH-)�����ݵ���غ�c(H+)+c(Na+)=c(OH-)+c(CH3COO-)����c(Na+)<c(CH3COO-)���ʴ�Ϊ��>��<��
��3���ټ���Һ��pH =11��c(H+)=10-11 mol/L��c(OH-) =10-3mol/L���ʴ�Ϊ��0.001��
�����ڰ�ˮ�����c(NH3H2O) >10-3mol/L��c(NaOH) =10-3mol/L������25��ʱ��������ļס�������Һ���Ũ�ȵ����ᷴӦ�����ĵ������������>�ң��ʴ�Ϊ��>��
�����ڰ�ˮ�����ϡ�����е���̶�����n(OH-)����NaOH��ǿ��ʼס�����Һ����ˮϡ��10����������Һ��pH����>�ң��ʴ�Ϊ��>��
��4��A .H2O2 +SO2=H2SO4����A��ȷ��
B. Na2CO3 +SO
C. Na2SO3 +SO2+H2O= 2NaHSO3����C��ȷ��
D Ca(OH)2+SO2= CaSO3��+H2O����D��ȷ��
��ѡABCD��
��5��A.���ݱ����ṩ�����ݿ�֪H2SO3�����Դ���HCO3-���ٸ���ǿ���������ԭ��������A����ȷ�ģ�
B. ���ݱ����ṩ���ݺ�ǿ���������ԭ��������B����ȷ�ģ�
C. HClO�ܰ�SO32-������SO42-����C����
D.���ݱ����ṩ�����ݿ�֪��������Դ���̼�ᣬ��D��ȷ��
��ѡABD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ȣ�ClO2����һ�����������������������ƣ�NaClO3��Ϊԭ���Ʊ���
��1����Ĥ��ⷨ�Ʊ�ClO2��װ��ʾ��ͼ���£�

��֪��ClO2��������Һ�бȽ��ȶ����ڼ�����Һ�в����ȶ����ڡ�
�ٲ���O2�ĵ缫��Ӧʽ��________��
�ڽ�Ϸ�Ӧ����ʽ������ClO2�IJ������̣�_________��
��2���������ԭ���Ʊ�ClO2��![]() �о�����Cl-��������Ӧ��Ӱ�죬ʵ���¼���£�
�о�����Cl-��������Ӧ��Ӱ�죬ʵ���¼���£�
����NaCl ��Ũ��/(g��L1) | ClO2����������/(g��L-1��min-1) | ��ͬʱ�� | |||
10 min | 30 min | 60 min | ClO2 ����/% | Cl2 ���� | |
0 | 0.0035 | 0.0124 | 0.0159 | 97.12 | ���� |
1.00 | 0.0138 | 0.0162 | 0.0163 | 98.79 | ���� |
��NaCl����Ҫ������_______��
��������Ӧ���ܵĹ������£�
��Ӧi��![]() +
+ ![]() + +
+ +
��Ӧii�� Cl2 + H2O2 = 2Cl- + O2�� + 2H+
����Ӧi��д����_________��
�۽�һ���о����֣�δ����Cl-ʱ����ϵ�����Ȼᷢ����Ӧ����Cl-����ӦΪ��ClO3- + 3H2O2 = Cl- + 3O2��+3H2O����Ӧiii����������Ӧi��ii��iii�����ʴ�С��ϵ����Ҫ˵�����ɣ�_________��
��3�����ҹ涨������ˮ��ClO2�IJ��������ø���0.8 mg��L-1����ⲽ�����£�
����ȡ1.0L������ˮ������������ĵ⻯�أ���������������Һ�������ԣ�ʹClO2ת��Ϊ![]() �����������Һ����Һ������
�����������Һ����Һ������
������0.0010 mol/LNa2S2O3��Һ�ζ�����I�в�����I2����֪������II�з�����Ӧ�����ӷ���ʽ��![]()
�ٲ���I�з�����������ԭ��Ӧ�����ӷ���ʽ��________��
�ڵ�����II�г���________��������ʱ��ֹͣ�μ�Na2S2O3��Һ����¼�����Ϊ10.00 mL��
������ˮ����ClO2�IJ���Ũ����______mg��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ֽС���άͪ����Һ������άͪͨ�������HI3�γɾ�άͪ�⣬��ṹ��ʾ��ͼ��ʾ������˵����ȷ����
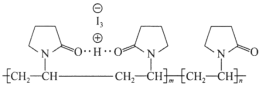 (ͼ�����߱�ʾ���)
(ͼ�����߱�ʾ���)
A.C��N��Oԭ�ӵĵ縺����������
B.��άͪ���к������Ӽ������ۼ�������Ȼ�ѧ��
C.��άͪ������ˮ��ԭ������ˮ���Ӽ��γ����
D.�����еĺ�N��Ԫ��һ����ƽ��ṹ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������н��з�ӦCH4(g)+H2O(g) ![]() CO(g)+3H2(g)�� ��H>0�����c(CH4)�淴Ӧʱ��(t)�ı仯��ͼ��ʾ�������ж���ȷ���ǣ� ��
CO(g)+3H2(g)�� ��H>0�����c(CH4)�淴Ӧʱ��(t)�ı仯��ͼ��ʾ�������ж���ȷ���ǣ� ��
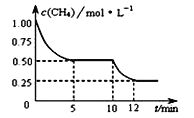
A. 10 minʱ���ı��������������������¶�
B. ��Ӧ���е�12minʱ��CH4��ת����Ϊ25%
C. 0��5 min�ڣ�v(H2)��0.1 mol��(L��min)-1
D. �����£���С���������ƽ���H2Ũ�ȼ�С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����W��X��Y��Z���ֽ���������װ�ý���ʵ�顣����˵������ȷ���ǣ� ��
װ�� |
|
|
|
���� | ����W�����ܽ� | Y���������� | W����������� |
A.װ�ü���X��ԭ�������
B.װ������Y�缫�ϵķ�ӦʽΪCu2++2e=Cu
C.װ�ñ�����Һ��c(H+)����
D.���ֽ����Ļ��ǿ��˳��ΪZ��W��X��Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�Ĺ�����Ŀǰֱ������̫���ܵ��о��ȵ㡣���ǰ�ͨ���˹��⻯ѧ�ֶκϳ�ȼ�ϵĹ��̽����˹�������á�
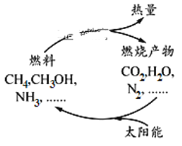
(1)����ͼ��������ʺ�����ѭ����̫��������ת��Ϊ____________�ܡ�
(2)�˹�������õ�;��֮һ�����ڴ������������£���CO2��H2Oת��ΪCH3OH���÷�Ӧ�Ļ�ѧ����ʽΪ��2CO2(g)+4H2O(g)![]() 2CH3OH(g)+3O2(g)��
2CH3OH(g)+3O2(g)��
һ�������£���2 L�ܱ������н���������Ӧ�����n(CH3OH)��ʱ��ı仯�����ʾ��
ʱ��/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
n(CH3OH)/mol | 0.000 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
����CH3OH��ʾ0��3 min�ڸ÷�Ӧ��ƽ����Ӧ����Ϊ______________________��
����˵���÷�Ӧ�Ѵﵽƽ��״̬����_______________��
a��v��(H2O)=2v��(CO2) b��n(CH3OH����n(O2)=2��3
c���������ܶȱ��ֲ��� d��������ѹǿ���ֲ���
(3)�ҹ���ѧ����Fe3(CO)12/ZSM-5��CO2����ϳɵ�̼ϩ����Ӧ�����ò��ﺬCH4��C3H6��C4H8�ȸ������Ӧ������ͼ��
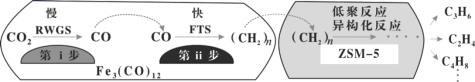
����������Na��K��Cu����������Ҳ������ã��ɸı䷴Ӧ��ѡ���ԣ�������������ͬʱ�����Ӳ�ͬ������������ͬʱ�����CO2ת���ʺ���������ʵ������������

������ߵ�λʱ������ϩ�IJ�������Fe3(CO)12/ZSM-5������____________����Ч����ã�
�ڼ�����������ߵ�λʱ������ϩ�����ĸ���ԭ����____________��
(4)���˹�������õõ��ļ״���������ϡ����������أ���״�Ӧͨ��õ�ص�____��(����������������)����Һ�е�H+����õ�ص�____��(����������������)ͨ��������һ���ĵ缫��ӦʽΪ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ����ȡ�屽��

(1)װ��A��������_______________��
(2)��ȡ�屽�Ļ�ѧ��Ӧ����ʽ_____________��
(3)��Ӧʱ��װ��B�г��ֵ�������___________��
(4)����ˮ˳��_______(A���Ͻ��³���B���½��ϳ�)�������ܵ�����____________�������װ��C�е���λ��Ϊʲô��������Һ������____________��
(5)װ��D��������__________��
(6)��Ӧ��������Һ©���е���ҺE���뵽��ƿB�У������ɳ�ȥ�屽�е��壬��ҺE��_______________��Һ�徭����Һ�����õ��屽�л���������������ν��з���________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ��س����ں��ϸ���������豸�У���ʾ��ͼ��ͼ��ʾ����ط�ӦΪ2Li��2H2O��2LiOH��H2������ع���ʱ������˵���������( )

A.�����������
B.���Ӵ�﮵缫�������������缫
C.��ˮ��Ϊ�������Һ
D.�ɽ�����ת��Ϊ��ѧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Դ�����þ��й���ǰ����
(1)��ͼ�ǴӺ�ˮ����ȡþ�ļ����̡�

�ٹ�ҵ�ϳ����ڳ���Mg2+���Լ�A��_____________��
������ˮMgCl2��ȡMg�Ļ�ѧ����ʽ��_______________��
(2)�������и�����I-��ʽ���ڵĵ�Ԫ�أ�ʵ������ȡI2��;��������ʾ��
�ɺ���![]() ������
������![]() ��Һ
��Һ![]()
![]() I2
I2
�����պ������ҽ�ʱ���õ���Ҫ����������___________ ��
�����ữ����Һ�мӹ���������Һ��д���÷�Ӧ�����ӷ���ʽ______________��
�۷�Ӧ��������CCl4����ȡ����������ȡ����Һ�ķ����ӵ�ˮ����ȡ�⣬��Ҫ����������ͼ��

�ס��ҡ���3��ʵ������У�����ȷ����_________ (������������������������)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com