
| A、300 mL 3.5 mol/L KCl溶液 |
| B、1 000 mL 2.5 mol/L NaCl溶液 |
| C、250 mL 1 mol/L AlCl3溶液 |
| D、200 mL 2 mol/L MgCl2溶液 |


科目:高中化学 来源: 题型:
| A、硒化氢是无色、有毒、比硫化氢稳定的气体 |
| B、砹单质是一种有色固体,砹化氢很不稳定,砹化银是难溶于水的白色沉淀 |
| C、硫酸锶难溶于水,但易溶于盐酸 |
| D、铍(Be)是一种轻金属,它的氧化物的水化物可能具有两性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
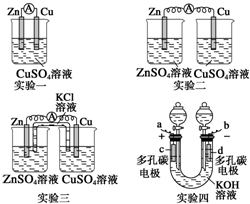 某校化学兴趣小组为了探究原电池工作原理,进行下列实验,请分析实验结果后回答相应问题.
某校化学兴趣小组为了探究原电池工作原理,进行下列实验,请分析实验结果后回答相应问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.37 mol |
| B、0.63mol |
| C、0.75mol |
| D、1.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯与溴反应制1,2-二溴乙烷 |
| B、苯酚与浓溴水反应生成三溴苯酚 |
| C、甲苯使酸性高锰酸钾溶液褪色 |
| D、在一定条件下苯与氢气反应制取环己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
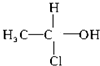 .下列化合物中存在对映异构体的是( )
.下列化合物中存在对映异构体的是( )| A、C2H5CH=CHCH(CH3)-CH=CHC2H5 |
B、 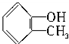 |
| C、甲酸 |
| D、C6H5CH(CH3)OCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向0.1 mol?L-1氯化铁溶液中加入少量的KOH溶液制取氢氧化铁胶体 |
| B、由0.1mol氯化铁制取的氢氧化铁胶体中,氢氧化铁胶粒数目小于0.1NA(设NA表示阿伏加德罗常数的值) |
| C、氢氧化铁胶体通电后氢氧化铁胶粒向正极移动 |
| D、可以用布朗运动区别硫酸铜溶液和氢氧化铁胶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com