
 如图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题。
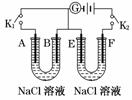
如图所示,A、F为石墨电极,B、E为铁片电极。按要求回答下列问题。
(1)打开K2,闭合K1,B为____________极,A的电极反应式为:____________________________________________________,
可观察到的现象是________。
(2)打开K1,闭合K2,E为________极,F极的电极反应式为:________ __________;检验F极产生气体的方法是________________________________。
__________;检验F极产生气体的方法是________________________________。
(3)若往U形管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是________,原因是______________________________________________。
解析:(1)当打开K2,闭合K1时,铁片、石墨和NaCl溶液构成原电池,负极为铁,电极反应式为:Fe-2e-===Fe2+,正极为石墨,由于电解质溶液呈中性,正极的电极反应式为:O2+4e-+2H2O===4OH-;由于Fe2++2OH-===Fe(OH)2↓,4Fe(OH)2+O2+2H2O===4Fe(OH)3,所以,可观察到的现象是:溶液中产生白色沉淀,然后变为灰绿色,最终变为红褐色。
(2)当打开K1,闭合K2时,铁片、石墨和NaCl溶液构成电解池,阴极为铁,电极反应式为:2H++2e-===H2↑,阳极为石墨,电极反应式为:2Cl--2e-===Cl2↑;检验Cl2的方法是:用湿润的淀粉-KI试纸检验,试纸变蓝则说明是氯气。
(3)由于A极O2得到电子产生OH-,E极上水放电产生H2和OH-,均导致电极区域呈碱性,所以A、E电极周围遇酚酞变红。
答案:(1)负 O2+4e-+2H2O===4OH- 溶液中产生白色沉淀,然后变为灰绿色,最终变为红褐色
(2)阴 2Cl--2e-===Cl2↑ 用湿润的淀粉-KI试纸检验,试纸变蓝则说明是氯气
(3)A、E A极上O2放电产生OH-,E极上水放电产生H2和OH-,均导致电极区域呈碱性


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下列物质之间的变化:

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中分离溶液和沉淀采用的相同的操作是________。
(2)写出下列B、C、D、E所含物质的化学式:固体B____________;沉淀C________;沉淀D________;溶液E________。
(3)写出①、②、③、④四个反应的化学方程式或离子方程式。
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________;
④________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在FeCl3、CuCl2混合溶液中,加入一定量的铁屑,反应完全后将固体滤出,下列说法中正确的是
A.若固体中只有铜,则溶液中一定含有Fe2+,一定不含Cu2+
B.若固体中只有铜,则溶液中一定含有Fe2+,可能含有Cu2+和Fe3+
C.若固体中只有铜,则溶液中一定含有Fe3+和Fe2+,一定不含Cu2+
D.若固体中含有铁和铜,则溶液中一定含有Fe2+,一定不含Cu2+和Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于电解的叙述中,正确的是( )
①电解是把电能转变成化学能 ②电解 是把化学能转变成电能 ③电解质溶液导电是化学变化,金属导电是物理 变化 ④某些不能自发进行的氧化还原反应,通过电解可以实现 ⑤任何水溶液电解时,必将导致氧化还原反应
是把化学能转变成电能 ③电解质溶液导电是化学变化,金属导电是物理 变化 ④某些不能自发进行的氧化还原反应,通过电解可以实现 ⑤任何水溶液电解时,必将导致氧化还原反应
A.②③④ B.①②③④
C.①②④ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
用下图Ⅰ所示装置通电10分钟后,去掉直流电源,连接成图Ⅱ所示装置,可观察到U形管左端铁电极表面析出白色胶状物质,U形管右端液面上升。下列说法正确的是( )
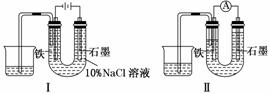
A.同温、同压下,装置Ⅰ中石墨电极上方得到的气体比铁电极上方得到的气体多
B.用装置Ⅱ进行实验时铁电极的电极反应为Fe-2e-+2OH-===Fe(OH)2
C.用装置Ⅱ进行实验时石墨电极的电极反应为2H++2e-===H2↑
D.装置Ⅰ通电10分钟后铁电极周围溶液pH降低
查看答案和解析>>
科目:高中化学 来源: 题型:
钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。请回答钢铁腐蚀与防护过程中的有关问题。
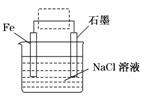
(1)钢铁的电化学腐蚀原理如图所示:
①写出石墨电极的电极反应式__________________________________________;
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在右图虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向。
③写出修改后石墨电极的电极反应式_________________________________。
(2)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式_____________ ________________________。
________________________。
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下:

①A电极对应的金属是________(写元素名称),B电极的电极反应式是________________________。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则 电镀时电路中通过的电子为________ mol。
电镀时电路中通过的电子为________ mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol·L-1Ba(OH)2溶液300 mL(忽略溶液体积变化),反应后溶液中SO 的物质的量浓度为( )
的物质的量浓度为( )
A.0.4 mol·L-1 B.0.3mol·L-1 C.0.2 mol·L-1 D.0.1 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com