
【题目】关于下列各装置图的叙述中,不正确的是 ( )
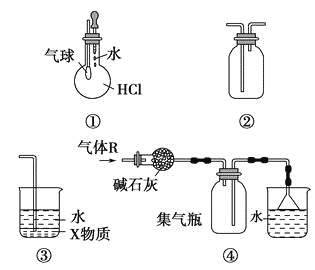
A.装置①可验证HCl气体在水中的溶解性
B.装置②可用于收集H2、NH3、Cl2、HCl、NO2、NO等
C.装置③中X为四氯化碳,可用于吸收氨气或氯化氢
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
科目:高中化学 来源: 题型:
【题目】丙烷是液化石油气主要成分之一,是一种优良的燃料。试回答下列问题:
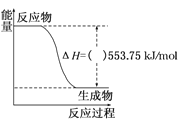
(1)如图是一定量丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,(图中的括号内填入“+”或“﹣”)_____。写出表示丙烷燃烧热的热化学方程式:_________________________
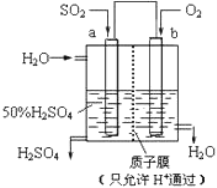
(2)科研人员设想用如图所示装置生产硫酸。
①上述生产硫酸的总反应方程式为_____________,b 是___________ 极(填“正”或“负”),b 电极反应式为______________________________,a 电极发生______________ (填“氧化反应”或“还原反应”)。②生产过程中H+向_____(填 a 或 b)电极区域运动。
(3)将两个铂电极插入氢氧化钾溶液中,向两极分别通入甲烷和氧气,可构成甲烷燃料电池,已知通入甲烷的一极为负极,其电极反应式为:_______________________。电池在放电过程中,溶液的pH值将______________ 。(填“下降”“上升”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用不同方法制得白色的Fe(OH)2沉淀。
(1)用未被氧化的FeSO4溶液与煮沸过的蒸馏水配制的NaOH溶液反应制备,制备过程中下列说法正确的是_______
A.用硫酸亚铁晶体配制上述FeSO4溶液时还需加入适量盐酸防止水解
B.除去蒸馏水中溶解的O2也可以采取振摇、静止的方法
C.生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液
D.FeSO4溶液上面加一层苯可以防止空气中氧气直接与溶液接触
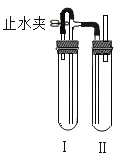
(2)在如图装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。在试管I 里加入稀H2SO4和铁屑,在试管II里加入NaOH溶液,打开止水夹,塞紧塞子,检验试管Ⅱ出口处排出的氢气的纯度。当排出的H2纯浄时,再____(填操作步骤),这样一段时间后试管Ⅲ中制得的Fe(OH)2沉淀能较长时间保持白色,其理由是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的铝土矿样品(主要成分为Al2O3,含Fe2O3杂质),加入100 mL稀硫酸中充分反应后向滤液中加入10 mol·L1NaOH溶液,产生沉淀的质量和加入NaOH溶液体积之间的关系如图所示。则所用硫酸物质的量浓度为( )
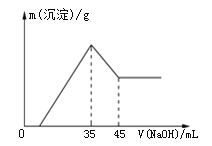
A.3.50 mol·L1B.0.85 mol·L1C.1.75 mol·L1D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法正确的是( )
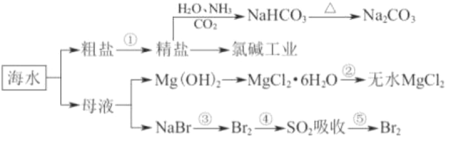
A. 工业上通过电解饱和MgCl2溶液制取金属镁
B. 第①步中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的药品顺序为NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
C. 在③、④、⑤步骤中,溴元素均被氧化
D. 制取NaHCO3的反应是利用其溶解度比较小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种主族元素X、Y、Z、M和N在周期表中的位置如图所示。下列说法正确的是

A. M的原子半径比N小
B. Y和Z既可形成Z2Y,也可形成Z2Y2
C. X2M的热稳定性比X2Y强
D. M和N的氧化物的水化物均为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由短周期元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)
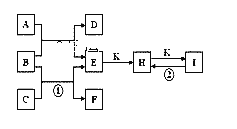
请回答下列问题:
(1)物质A的化学式为________;物质D的名称________;
(2)化合物I的化学式为_____________________;
(3)反应①的化学方程式为_______________________________________;
反应②的化学方程式为_______________________________________;
A与B反应的化学方程式________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若W原子最外层电子数与其内层电子数之比为7∶10,下列说法中不正确的是( )
![]()
A.最高价氧化物对应水化物的酸性:Y>Z
B.Y元素的两种同素异形体在常温下都是气体
C.原子半径由大到小排列顺序:Z>X>Y
D.阴离子半径由大到小排列顺序:Z>W>X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体的组成可表示为H2C2O4·xH2O,为测定x值,进行下述实验:
实验1:准确称取Wg草酸晶体配成100ml水溶液;
实验2:用浓度为0.100molL-1KMnO4溶液滴定所配制的草酸溶液,所发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+ 10CO2↑+2MnSO4+8H2O。
试回答下列问题:
(1)实验1中,配制100ml草酸水溶液所需要的一组仪器是________(填相应编号)
A、0.001g的电子天平 B、50ml酸式滴定管 C、100ml量筒 D、100ml容量瓶 E、烧杯 F、胶头滴管 G、锥形瓶
(2)实验2中H2C2O4·xH2O中x值的测定是利用氧化还原反应滴定法
①其中正确操作步骤的顺序为___________
a.用移液管取用25.00ml所配的草酸溶液置于锥形瓶中,加适量的稀硫酸。
b.把盛有KMnO4标准液的滴定管固定好,调节滴定管尖嘴使之充满液体
c.取KMnO4标准液注入滴定管中至“0”刻度以上
d.调节液面至“0”或“0”刻度以下,记下读数
e.把标准KMnO4溶液润洗滴定管2~3次
f.把锥形瓶放在滴定管下面,用KMnO4标准液滴定至终点并记下滴定管的读数
②下列关于滴定分析,正确的是________________。
A. 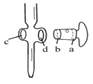 图中,应将凡士林涂在旋塞的a端和旋塞套内的c端
图中,应将凡士林涂在旋塞的a端和旋塞套内的c端
B. 滴定前,锥形瓶和滴定管均须用标准溶液润洗
C. 将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
D. 滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
E. 滴定到终点时俯视读取数据,测得的x值偏大
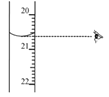
③图中滴定终点时显示的读数为_______ mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com