
| A. | 1:1 | B. | 1:5 | C. | 1:9 | D. | 2:3 |
分析 pH=13的氢氧化钠溶液与pH=2的硫酸溶液混合后溶液pH=11,说明NaOH过量,混合后溶液pH=11,则c(OH-)=0.001moL/L,根据c(OH-)=$\frac{n(O{H}^{-})-n({H}^{+})}{{V}_{酸}+{V}_{碱}}$计算.
解答 解:pH=13的氢氧化钠溶液中c(OH-)=0.1mol/L,pH=2的硫酸溶液c(H+)=0.01mol/L,
溶液混合后溶液pH=11,说明NaOH过量,混合后溶液pH=11,则c(OH-)=0.001moL/L,
设氢氧化钠的体积为xL,硫酸的体积为yL,
则 $\frac{0.1x-0.01y}{x+y}$=0.001,
x:y=1:9,
故选C.
点评 本题考查酸碱混合的计算,题目难度不大,本题注意从质量守恒的角度结合相关计算公式计算该题.


科目:高中化学 来源: 题型:选择题
| A. | Al3+、S2-、Na+、Cl- | B. | K+、Fe3+、S2-、OH- | ||
| C. | Ba2+、HCO3-、Fe3+、H+ | D. | Na+、Al3+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
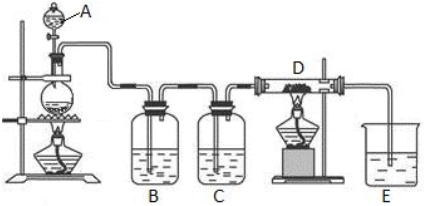
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6CO2(g)+6H2O(l)═C6H12O6(葡萄糖,s)+6O2(g)△H=-1880 kJ•mol-1 | |
| B. | 6CO2(g)+6H2O(l)═C6H12O6(葡萄糖,s)+6O2(g)△H=+2880 kJ•mol-1 | |
| C. | 6CO2(g)+6H2O(l)═C6H12O6(葡萄糖,s)+6O2(g)△H=+2560 kJ•mol-1 | |
| D. | 6CO2(g)+6H2O(l)═C6H12O6(葡萄糖,s)+6O2(g)△H=-1720 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 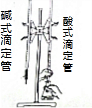 用HF标准溶液测定未知浓度的NaOH溶液 用HF标准溶液测定未知浓度的NaOH溶液 | |
| B. | 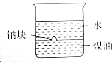 验证密度:ρ(水)<ρ(钠)<ρ(煤油) 验证密度:ρ(水)<ρ(钠)<ρ(煤油) | |
| C. | 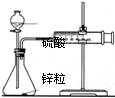 测定锌与硫酸反应的速率 测定锌与硫酸反应的速率 | |
| D. | 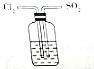 验证SO2和Cl2等物质的量混合增强漂白效果 验证SO2和Cl2等物质的量混合增强漂白效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3和Na2CO3均能和BaCl2反应 | |
| B. | NaHCO3和Na2CO3都能加热分解,产生使石灰水变浑浊的气体 | |
| C. | 质量相同的NaHCO3和Na2CO3分别与足量稀盐酸反应,NaHCO3放出气体多 | |
| D. | 可以用澄清石灰水来鉴别Na2CO3NaHCO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com