
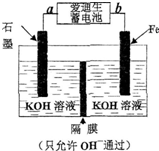
 �����仯�����Ϊ��Ҫ������ش���������
�����仯�����Ϊ��Ҫ������ش���������| Fe2O3 | CO | Fe | CO2 | |
| ��/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| ��/m01 | 1.0 | 1.5 | 1.0 | 1.0 |
| �ŵ� |
| ��� |
| c 3(CO2) |
| c 3(CO) |
| (1.6mol/2L) 3 |
| (0.4mol/2L)3 |


 ����ѧ����ϵ�д�
����ѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڻ�̬����ӵ�ԭ���У�����ʧȥ�ĵ���������ߵ�����Ҳ��С |
| B����ĵ�һ�����ܸ���̼���縺�Ե���̼ |
| C��PH3���ӳ������Σ��е��NH3�� |
| D��SiF4��SO32-������ԭ�Ӿ�Ϊsp3�ӻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� ��ȡ���� |
B�� ��ȥ�����е������Ȼ��� |
C�� ����������̺��Ȼ�����Һ |
D�� �����Ȼ�����Һ��MnCl2?4H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ũ��ˮ�м�����ʯ�ҿ�����ȡ������NH3 | ||||
B���ö��Ե缫�������NaCl��2Cl-+2H2O
| ||||
| C����ˮ�ͻ���̿ʹ��īˮ��ɫ������ͬһԭ������ | ||||
| D��Ũ�����Ũ���᳤�ڱ�¶�ڿ�����Ũ�ȶ��ή�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��FeCl2 |
| B��Na2SO3 |
| C��NaOH |
| D��AlCl3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� ��ȥ�Ҵ��е����� |
B�� �γ�ԭ��� |
C�� ��ȡ�������� |
D�� ʯ�͵ķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ӧ������ѹǿ����ʱ��仯 |
| B��������SO2��O2��SO3�����ʵ���֮��Ϊ2��1��2 |
| C��SO2��SO3��Ũ����� |
| D��������SO2��O2��SO3���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A | B | C | D | |
| ���� | ��Һ©�� | 250 mL����ƿ | ��ʽ�ζ��� | ������ |
| ͼ�� | 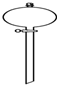 |  |  |  |
| ��; ��ʹ �ò� ���� | �þƾ���ȡ��ˮ�еĵ⣬��Һʱ���������Ͽڵ��� | ����1.0 mol?L-1 NaCl��Һ������ʱ���ӿ̶ȣ�����õ���ҺŨ�ȴ���1.0 mol?L-1 | ��������ȡ10.00 mL KMnO4��Һ | ����ʵ���н���������ΪҺ�� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com