
|
下图表示三种原子的原子结构:
其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的组合是 a、①②③互为同位素 b、①②③互为同素异形体 c、①②③是三种化学性质不同的粒子 d、①②③具有相同的质量数 e、①②③具有相同的质量 f、①②③是三种不同的原子 | |
| [ ] | |
A. |
af |
B. |
bc |
C. |
de |
D. |
ef |
科目:高中化学 来源:2007年全国普通高校统一招生考试(山东卷)理科综合试测题化学部分 题型:022
氢原子能与许多元素化合形成化合物.下图中,●代表原子序数在1到10之间的原子实(原子实是原子除去价电子后剩余的部分),小黑点“·”代表未成键价电子,短线代表一个化学键(如H2O表示为![]() ).
).

①写出A、B两种分子的结构式并推测其立体结构.
②C、D与A具有相似的分子结构,且A、C、D三种分子的中心原子属于同族非金属,试推测由A、C、D构成的三种纯净物中沸点最高的是哪一种?为什么?
查看答案和解析>>
科目:高中化学 来源: 题型:
单质A、B、C在常温下均为气态,分别由甲、乙、丙三种短周期元素组成;已知丙元素的原子结构中次外层电子数比最外层电子数多l,化合物D在常温下呈液态,G是常见的金属单质,H是常见的蓝色沉淀。各物质间的转化关系如下图所示(反应条件多数已略去);
请回答:
(1)反应⑥的离子方程式是
(2)甲、乙两元素除形成化合物D外,还可形成一种含有4个原子核和18个电子的化合物,该化合物的电子式是
(3)在反应①中,已知lgB,完全燃烧生成液态D时,放出142.9KJ的热量,则表示B燃烧热的热化学方程式是
(4)反应①也可以设计成原电池装置进行,当用铂作电极,用KOH溶液作电解质溶液时,负极的电极反应式是
(5)反应③④在通常情况下不能自发进行,框图中的条件a是 ,在使反应③④能够发生的装置中,有一个电极材料必须相同,写出该电极反应式
查看答案和解析>>
科目:高中化学 来源: 题型:
有关元素A、B、C、D、E的信息如下:
| 元素 | 有关信息 |
| A | 元素主要化合价为-2,A的一种氢化物可用于实验室制取A的单质 |
| B | 所在主族序数与所在周期序数之差为4 |
| C | 原子中含10个P电子 |
| D | 最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
| E | 生活中常见金属,它有两种氯化物,相对原子质量相差35.5 |
请回答下列问题:
 (1)元素A~E中两种元素组成的化合物使品红溶液褪色的物质的化学式为______。
(1)元素A~E中两种元素组成的化合物使品红溶液褪色的物质的化学式为______。
(2)E元素与B元素可形成EB2和EB3两种化合物,下列说法正确的是(填序号)________。
①保存EB2溶液时,需向溶液中加入少量E单质
②EB2只能通过置换反应生成,EB3只能通过化合反应生成
③铜片、碳棒和EB3溶液组成原电池,电子由铜片沿导线流向碳棒
④向淀粉碘化钾溶液和苯酚溶液中分别滴加几滴EY3的浓溶液,原无色溶液都变为紫色
(3)用化学符号表示D2C的水溶液中各粒子的浓度关系,如c(C2-)=______________。
(4)将一定量的B单质通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中含有三种含B元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化示意图如下图所示。该苛性钾溶液中KOH的质量是___________,该反应中转移电子的物质的量是_________。
(5)工业上冶炼E单质的化学方程式为__________________________________。
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题
 ”代表未成键价电子,短线代表一个化学键。
”代表未成键价电子,短线代表一个化学键。

查看答案和解析>>
科目:高中化学 来源: 题型:
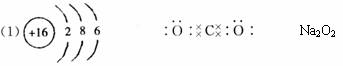
请回答:
(1)写出C元素的原子结构示意图___________________,写出丁的电子式______________,写出戊的化学式_____________________________。
(2)乙溶液呈酸性的原因是(用电离方程式表示)___________________;丙溶液呈碱性的原因是(用离子方程式表示)______________________________。
(3)写出反应的离子方程式:已溶液+丙溶液→丁:___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com