
科目:高中化学 来源: 题型:
【题目】下列各组中,两种气体的分子数一定相等的是 ( )
A. 温度相同、体积相同的O2和N2 B. 体积相等、密度不等的CO和C2H4
C. 质量相等、密度不等的CO和C2H4 D. 压强相同、体积相同的O2和N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼系高温超导材料都具有良好的应用前景。回答下列问题:
(1)B的基态原子价电子排布式为____________________。BF3的立体构型是_____________________。
H3BO3为一元酸,与足量NaOH溶液反应得到[B(OH)4 ]-,[B(OH)4]-中B的杂化轨道类型为__________________________。
(2)NaBH4被认为是有机化学上的“万能还原剂”,NaBH4的电子式为_________________,其中三种元素的电负性由大到小的顺序是__________________________。
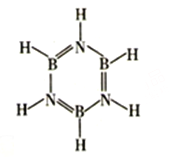
(3)硼与氮形成类似苯的化合物硼氮苯(B3N3H6),俗称无机苯(如图)。硼氮苯属于____________(填“极性”或“非极性”)分子,其间位上的二氯代物有______________种.
(4)NH4BF4 (氟硼酸铵)是合成氮化硼纳米管的原料之一。1mol NH4BF4含有_________mol 配位键。
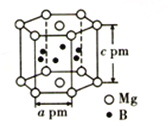
(5)硼与镁形成的高温超导材料晶体结构如图所示(B在六棱柱柱体内)。该六方晶胞中镁原子与硼原子的数量比为_____________,晶体密度d=_______________g·cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期金属元素甲~戊在周期表中的相对位置如表所示,下面判断不正确的是( )
甲 | 乙 | |
丙 | 丁 | 戊 |
A.原子半径:丙>丁>戊
B.最外层电子数:甲>乙
C.金属性:甲<丙
D.氢氧化物碱性:丙>丁>戊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜-锌原电池,电解质溶液为稀硫酸,当该原电池工作时
A. 铜电极发生氧化反应 B. 铜电极发生还原反应
C. 电子由铜极经外电路流向锌极 D. 电解质溶液中的H+浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期主族元素原子半径与原子序数的关系图。下列说法正确的是( )
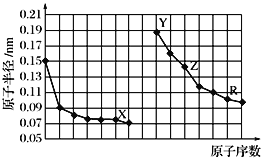
A. Z和R所形成的化合物,不能通过溶液中复分解反应而制得
B. 简单离子的半径关系是:R>Y>Z>X
C. X和Y所形成的一种化合物,可用于自来水消毒
D. 工业上获得单质Z的方法,一般是通过电解其熔融氯化物来实现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学发现一瓶失去标签的药品,取出少量,观察到该药品为白色固体,加入蒸馏水后,发现白色固体全部溶解,他认为该药品有可能是钠的化合物,需要用焰色反应来进一步验证。上述过程没有用到的科学探究方法是( )
A.假设法B.观察法C.比较法D.实验法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产硫酸需经过SO2的制造、SO2的催化氧化和SO3的吸收三个主要阶段,下列说法错误的是( )
A.废渣可做建材B.将矿石粉碎增大反应速率
C.尾气直接排放D.热交换器提高能量利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,1mol·L-l的某二元酸H2A溶液中,存在的HA-、A2-的物质的量分数随pH变化的关系如图所示,
下列说法不正确的是
A. H2A的电离方程式为:H2A==H++HA- HA-![]() A2-+H+
A2-+H+
B. 室温下,电离平衡HA-![]() A2-+H+的平衡常数Ka=10-3。
A2-+H+的平衡常数Ka=10-3。
C. 等物质的量浓度NaHA和Na2A溶液等体积混合,离子浓度大小关系为:c(Na+)>c(HA-)>c(A2-)
D. 在Na2A溶液中存在c(Na+)=2c(A2-)+2c(HA-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com