
�мס��ҡ����������ʣ�
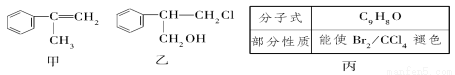
��1�����к��еĹ����ŵ�����Ϊ________��
��2���ɼ�ת��Ϊ���辭���й���(����ȥ������Ӧ���ز����ͬ)��

���з�Ӧ��ķ�Ӧ������______________����Ӧ���������__________________����Ӧ��Ļ�ѧ����ʽΪ_________________(����ע����Ӧ����)��
��3���ɼ׳����ϳɱ���·��֮һ����
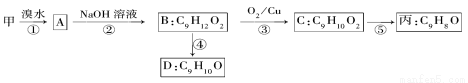
���������ʲ�����B��Ӧ����________(����ĸ)��
a�������� b��FeCl3  c��̼������Һ d��HBr
c��̼������Һ d��HBr
�ڱ��Ľṹ��ʽΪ______________��
��D������������������ͬ���칹��________�֣���д����һ����ͬʱ��������������ͬ���칹��ṹ��ʽ��___________��
a�������ϵ�һ�ȴ��������� b����FeCl3��Һ������ɫ��Ӧ c������Br2/CCl4��Һ��Ӧ
 �㽭�¿γ���άĿ�������ʱ��ѵϵ�д�
�㽭�¿γ���άĿ�������ʱ��ѵϵ�д� ��������ϵ�д�
��������ϵ�д� ���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
���ɶ���ܲ��¿�ֱͨ�߿�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������������ѧ��У����һ��6�¿���ѧ���������棩 ���ͣ�������
��30g������46g�Ҵ���Ӧ�����ʵ�ʲ��������۲��ʵ�67%����ʵ����������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������������ѧ��У���߶���6�¿���ѧ���������棩 ���ͣ�ѡ����
���з���������ԭ��һ������ͬһƽ����� �� ��
A��CH2��CH��C��C H B��CH2��CH��CH��CH2
H B��CH2��CH��CH��CH2

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ����5�¸߿�����һģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��ҵ�Ͽ���A�ͻ���ϩ( )Ϊԭ�Ϻϳ�ij��Ҫ���л���X��Y��·������(���ַ�Ӧ������)��
)Ϊԭ�Ϻϳ�ij��Ҫ���л���X��Y��·������(���ַ�Ӧ������)��

��1��B�к��������ŵ�������___________��
��2��A�Ľṹ��ʽ��______________��
��3����ѡ1�־��з�ʽ�ṹ��C��ͬϵ��ýṹ��ʽ��ʾ�䷴ʽ�ṹ_______��
��4����Ӧ�ڡ��ۡ��ܡ������뷴Ӧ�ٵ�������ͬ����_________��
��5��G��H�Ļ�ѧ����ʽ��__________��
��6��E�Ľṹ��ʽ��________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ����5�¸߿�����һģ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йص������Һ������Ũ�ȹ�ϵ��ȷ����
A��pH=a�Ĵ�����Һ��ϡ��10������pH=b����a=b-1
B���������ʵ�����NaHSO3��Na2SO3����Һ��2c(Na+)=3[c(HSO3-)+c(SO32-)+c(H2SO3)]
C��0.1mol��L-1������0.2mol��L-1��ˮ�������ϣ�c(NH3��H2O)>c(Cl-)>c(NH4+)>c(OH-)
D������AgCl��AgI���������Һ��c(Ag+)>c(Cl-)=c(I-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������������и���5����Ӧ��ѵ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�о�NO2��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1����֪��2SO2(g)+O2(g)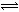 2SO3(g) ��H=-196.6 kJ��mol��1��2NO(g)+O2(g)
2SO3(g) ��H=-196.6 kJ��mol��1��2NO(g)+O2(g)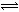 2NO2(g) ��H=-113.0 kJ��mol��1����Ӧ��NO2(g)+SO2(g)
2NO2(g) ��H=-113.0 kJ��mol��1����Ӧ��NO2(g)+SO2(g)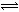 SO3(g)+NO(g)�Ħ�H= kJ��mol��1
SO3(g)+NO(g)�Ħ�H= kJ��mol��1
��2�����÷�Ӧ6NO2�� 8NH3 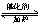 7N2��12H2O�ɴ���NO2��һ�������£����÷�Ӧ��Ƴ�����ͼ��ʾװ�ã����е缫��Ϊʯī��ʹ�����ڽ���������������ʣ�д�������缫��Ӧʽ ����һ��ʱ���ڲ�����·����1.2mol����ͨ��������������������������ڱ�״���µ����Ϊ L��
7N2��12H2O�ɴ���NO2��һ�������£����÷�Ӧ��Ƴ�����ͼ��ʾװ�ã����е缫��Ϊʯī��ʹ�����ڽ���������������ʣ�д�������缫��Ӧʽ ����һ��ʱ���ڲ�����·����1.2mol����ͨ��������������������������ڱ�״���µ����Ϊ L��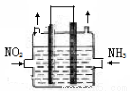
��3��һ�������£���NO2��SO2�������1�U2���ں����ܱ������з���������Ӧ��NO2(g)+SO2(g)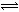 SO3(g)+NO(g)��������˵���÷�Ӧ�ﵽƽ��״̬���� ��
SO3(g)+NO(g)��������˵���÷�Ӧ�ﵽƽ��״̬���� ��
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c��SO3��NO�����ʵ����ȱ��ֲ��� d��ÿ����1 mol SO3��ͬʱ����1 molNO2
��4��CO�����ںϳɼ״�����Ӧ����ʽΪ��CO(g)+2H2(g)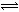 CH3OH(g)��һ���¶��£����ݻ�Ϊ2L���ܱ������г���2molCO��2molH2��������
CH3OH(g)��һ���¶��£����ݻ�Ϊ2L���ܱ������г���2molCO��2molH2�������� ��Ӧ��5min��Ӧƽ�⣬��ʱ���CH3OH��Ũ��Ϊ0.3mol/L�����㷴Ӧ��ʼ��ƽ��ʱ��ƽ������v(H2)= �����¶��·�Ӧ��ƽ�ⳣ��Ϊ (������λС��)��
��Ӧ��5min��Ӧƽ�⣬��ʱ���CH3OH��Ũ��Ϊ0.3mol/L�����㷴Ӧ��ʼ��ƽ��ʱ��ƽ������v(H2)= �����¶��·�Ӧ��ƽ�ⳣ��Ϊ (������λС��)��
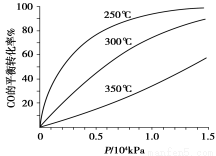
��5����ͬ�¶�CO��ƽ��ת������ѹǿ�Ĺ�ϵ����ͼ��ʾ���÷�Ӧ��H 0���>���� <������ʵ����������������250�桢1.3��104kPa���ң�ѡ���ѹǿ�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������������и���5����Ӧ��ѵ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ѧ������������أ�����˵����ȷ����
A�������г����ȵ�С�մ�ȥ�ۣ�������ˮ�����ȵ��ص�
B��Mg���ɵ��MgCl2ˮ��Һ��ȡ��Al���ɵ������Al2O3��ȡ
C�������̷����߲˱����������������֣����ӳ�����ʱ��
D��SiO2�����������������SiO2����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�����и�һ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�����ܱ������еķ�Ӧ��N2(g)+3H2(g) 2NH3(g)��673K��30MPa��n(NH3)��n(H2����ʱ��仯�Ĺ�ϵ����ͼ��ʾ������������ȷ���ǣ� ��
2NH3(g)��673K��30MPa��n(NH3)��n(H2����ʱ��仯�Ĺ�ϵ����ͼ��ʾ������������ȷ���ǣ� ��
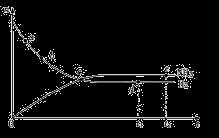
A����a������Ӧ���ʱȵ�b��С
B����c����Ӧ�ﵽƽ��
C����d (t1ʱ�̣��͵�e (t2ʱ�̣���n (N2����һ��
D�������������䣬773K�·�Ӧ��t1ʱ�̣�n(H2)��ͼ��d���ֵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡɳ�и����߿�ǰ���һ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�л���M 7.4 g������������Ӧ��������������ͨ��ʢ��ŨH2SO4�ͼ�ʯ�ҵ�װ�ã���װ�÷ֱ�����9 g��17.6 g��ͬ��ͬѹ�£�M�������ܶ���H2��37�������ܹ����Ʒ�Ӧ�ų�H2��M��ͬ���칹�����Ŀ�������������칹��
A��8 B��6 C��4 D��2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com