
| A. | 不同的催化剂对化学反应速率的影响均相同 | |
| B. | 哈伯法合成氨是吸热反应,新法合成氨是放热反应 | |
| C. | 新法合成能在常温下进行是因为不需要锻炼化学键 | |
| D. | 新法合成与哈伯法相比不需要在高温条件下,可节约大量能源,极具发展愿景 |
分析 A.不同的催化剂催化机理不同,效果也不同;
B.两个化学反应都是放热反应;
C.化学反应的实质是旧化学键的断裂和新化学键的形成;
D.高温条件需要大量能源;
解答 解:A.不同的催化剂催化机理不同,效果也不同,但在其他条件相同时,转化率是一样的,故A错误;
B.新法合成与哈伯法合成都是反应物总能量大于生成物总能量,所以都是放热反应,只是新法降低了反应所需的能量,减少能源消耗,故B错误;
C.新法实际上是降低了反应所需的能量,旧化学键要断裂、新化学键也同时生成,反应的本质与催化剂无关,故C错误;
D.高温条件需要大量能源,用transFe(DMeOPrPE)2Cl2作催化剂,在常温常压下合成出氨,减少能源消耗,所以新法合成与哈伯法相比不需要在高温条件下,可节约大量能源,极具发展远景,故D正确;
故选D.
点评 本题考查催化剂对化学反应的影响,催化剂能通过改变活化能而影响反应速率,但不影响平衡移动,为易错题.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制一定物质的量的浓度的溶液时,定容时仰视刻度线会导致所配溶液浓度偏低 | |
| B. | 用托盘天平秤取25.20g NaCl | |
| C. | 用100mL 量筒量取5.2mL 盐酸 | |
| D. | 用浓盐酸配制一定物质的量浓度的稀盐酸,将量取的浓盐酸倒入容量瓶中,加水稀释到刻度线即可 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3Fe+4H2O(g)═Fe3O4+4H2 | B. | 2Na+2H2O═2NaOH+H2↑ | ||
| C. | 2F2+2H2O═4HF+O2? | D. | Cl2+2H2O═HClO+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L0.1mol/L的 Na2S溶液中S2-的个数为0.1NA | |
| B. | 标准状况下,11.2LH2所含的中子数为0.15 NA | |
| C. | 7.8g Na2O2与足量的水反应,转移的电子数为0.2 NA | |
| D. | 1mol羟基所含电子数为9 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 现象或事实 | 解释或解决方法 |
| A | 大量的燃煤、燃油是形成雾霾的主要原因, | 发展核能等清洁能源,减少化石燃料的使用 |
| B | “地沟油”是被氧化、分解的油脂,禁止食用 | 采用化学技术处理后代替汽油作燃料 |
| C | 氢氧化钠与氢氟酸都能与硅、二氧化硅反应 | 硅、二氧化硅都具有两性 |
| D | 漂白粉在空气中久置变质是 | 漂白粉中的有效成分与空气中的CO2反应生成CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
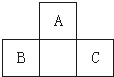 A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )
A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )| A. | Be、Na、Al | B. | B、Mg、Si | C. | C、Al、P | D. | O、P、Cl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com