
| 3 |
| 4 |
| 3 |
| 4 |
| 3 |
| 4 |
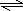 NH3?H2O+H+��������Ũ��������H+�������SO42-���ٴ���NH4+��OH-��С��ZΪHNO3��XΪNH4NO3��
NH3?H2O+H+��������Ũ��������H+�������SO42-���ٴ���NH4+��OH-��С��ZΪHNO3��XΪNH4NO3��| 10-14 |
| 10-a |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͬ���£�HF��HClO���룬���Ũ�ȵ����NaF��Һ��pH��NaClO��Һ��pH�� |
| B�������£�0.4mol?L-1 HA��Һ��0.2mol?L-1 NaOH��Һ�������Ϻ��pH����3��������Һ������Ũ�ȴ�С��ϵ��c��A-����c��Na+����c��HA����c��H+����c��OH-�� |
| C��������pH=a��Al2��SO4��3��Һ��pH=a��H2SO4��Һ�У�ˮ�����c��H+����� |
| D���ò��缫���ʳ��ˮ��һ��ʱ��������������������Ϊ3��2��ͬ�����£���Ϊ�����Һ�ָ�ԭ״����ֻ������Һ��ͨ��һ������HCl���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��25��ʱ����AgClˮ��Һ�м������ᣬKspֵ��� |
| B��25��ʱ����CaCO3������Һͨ��CO2���г������� |
| C��25��ʱ��AgClˮ��Һ�У�c��Ag+����c��Cl-���ij˻���һ������ |
| D��25��ʱ����Mg��OH��2������Һ�м���������NH4Cl���壬c��Mg2+������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | һԪ�� | NaOH | �����Һ��pH |
| �� | c��HX��=0.1mol/L | c��NaOH��=0.1mol/L | pH=9 |
| �� | c��HY��=c1mol/L | c��NaOH��=0.1mol/L | pH=7 |

| �� �� | 250�� | 300�� | 350�� |
| �� | 2.041 | 0.270 | 0.012 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�鲽�� | ʵ������ |
| 1����þ����ɰֽ��ĥ�����ˮ�У�������Һ�еμӷ�̪��Һ | A������ˮ���ϣ��۳�С�����������˶�����֮��ʧ����Һ��ɺ�ɫ�� |
| 2�������Ƶõ�Na2S��Һ�еμ��������Ƶ���ˮ | B���������������Һ���dz��ɫ |
| 3����һС������Ʒ�����з�̪��Һ����ˮ�� | C�����ҷ�Ӧ������������ɫ���壮 |
| 4����þ��Ͷ��ϡ������ | D����Ӧ��ʮ�־��ң�������ɫ���� |
| 5��������Ͷ��ϡ������ | E�����ɵ���ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 3 |
| 2 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Cu2+��Na+��SO42-��Cl- |
| B��K+��Na+��HCO3-��NO3- |
| C��Ba2+��Na+��OH-��Cl- |
| D��OH-��SO32-��Ca2+��Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Al��Cu��ϡH2SO4���ԭ��أ��为����ӦʽΪ��Al��Al3++3e- |
| B����Mg��Al��NaOH��Һ���ԭ��أ��为����ӦʽΪ��Al+4OH��-Al��OH��4-+3e- |
| C����Fe��Cu��FeCl3��Һ���ԭ��أ��为����ӦʽΪ��Cu��Cu2++2e- |
| D����Al��Cu��Ũ�������ԭ��أ��为����ӦʽΪ��Cu��Cu2++2e- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com