
【题目】将4.0 mol PCl3和2.0 mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)![]() PCl5(g)。达到平衡时,PCl5为0.8mol,如果此时移走2.0molPCl3 和1.0mol Cl2,在相同温度下再达到平衡时PCl5的物质的量是
PCl5(g)。达到平衡时,PCl5为0.8mol,如果此时移走2.0molPCl3 和1.0mol Cl2,在相同温度下再达到平衡时PCl5的物质的量是
A. 0.8mol B. 0.4mol C. 小于0.4mol D. 大于0.4mol,小于0.8mol
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下,铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸
B.包装食品里常有硅胶、石灰、还原铁粉三类小包,其作用相同
C.浓硫酸可用于干燥H2S和CO2
D.合金的物理性质一般与其各组分金属的物理性质相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日本,金刚烷胺一直作为帕金森病的治疗药,并于1998年被批准用于流感病毒A型感染性疾病的治疗,金刚烷胺的合成路线如图所示。下列说法不正确的是

A. 金刚烷胶的分子式是C10H17N B. 金刚烷胺的一溴代物有四种
C. 该路线中的反应都属于取代反应 D. W的同分异构体中一定含有苯环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸锶可用于制造烟火及信号弹等。工业级硝酸锶[含Ca(NO3)2、Ba(NO3)2等杂质]的提纯流程如下。(已知:硝酸锶、硝酸钡不溶于浓硝酸)

(1)要加快“酸浸”速率所采取的措施是______(写一条即可)。
(2)操作1的名称是_______,洗涤所用的洗涤剂是______ .
(3)“滤液2”中过量的H2CrO4被N2H4还原为Cr3+,同时放出无污染的气体,写出发生反应的离子方程式______;氧化产物与还原产物的物质的量之比为______ 。
(4)已知Cr(OH)3不溶于水,还原后调节pH=8的目的是_______ 。
(5)为了测定“残渣2”中Cr元素的质量分数,进行以下实验。(已知:I2+2S2O32-=2I-+S4O62-)
![]()
①“残渣2”中Cr元素的质量分数为______(用代数式表示)。
②若加入的HI溶液过量太多,测定结果会是_____(填“偏高”、“偏低”或“无影响”),其原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以有机物X为原料合成聚酯类高分子化合物H的路线如下: 
已知:
回答下列问题:
(1)X中宫能团的名称为______,Y→Z的反应类型为_______。
(2)H的结构简式是______ 。
(3)W与NaOH水溶液反应的化学方程式为_______ 。
(4)M在一定条件下还可以合成含有六元环状结构的G,其反应方程式为______ 。
(5)满足下列条件的Z的同分异构体有______种(不考虑立体异构)。
①含有1个六元碳环,且环上相邻4个碳原子上各连有一个取代基
②1mol该物质与新制的Cu(OH)2悬浊液反应产生2mol砖红色沉淀
(6)参照题中合成路线图,设计以![]() 为原料(其它无机试剂任选)制备化合物
为原料(其它无机试剂任选)制备化合物 的合成路线如下:
的合成路线如下:
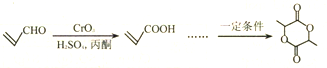 请把路线图中“……”补充完整____________________________。
请把路线图中“……”补充完整____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】面对目前世界范围内的能源危机,甲醇作为一种较好的可再生能源,具有广泛的应用前景。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g) ![]() CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH2=-41 kJ·mol-1
CO2(g)+H2(g) ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式:_______________________。
(2)在容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡时的转化率与温度、压强的关系如图所示。

①p1________p2(填“大于”、“小于”或“等于”);
②在温度和容积不变的情况下,再增加a mol CO与2a mol H2,达到新平衡时,CO的转化率________(填“增大”、“减小”或“不变”,下同),平衡常数________。
(3)关于CO(g)+2H2(g) ![]() CH3OH(g) ΔH1=-90 kJ·mol-1 正确的是_____________________
CH3OH(g) ΔH1=-90 kJ·mol-1 正确的是_____________________
A.温度和压强一定时,混合气体的密度不再变化,证明已经达到平衡状态
B. 2V(CO)正= V(H2)逆
C.温度和体积一定时,容器内压强不变,证明已经达到平衡状态
D.百分比组成2W(CO)=W(H2),证明已经达到平衡状态
E.混合气体的平均相对分子质量不再改变的状态,证明已经达到平衡状态
F.温度越高越有利于该反应自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F( )为一种高分子树脂,物质C的分子式为:C10H10Obr2;F的合成路线如下:
)为一种高分子树脂,物质C的分子式为:C10H10Obr2;F的合成路线如下:

已知:①A为苯甲醛的同系物,分子中无甲基,其相对分子质量为134;
②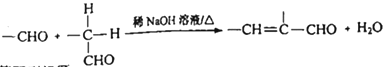
请回答下列问题:
(1)X的化学名称是_____________________________________。
(2)E生成F的反应类型为___________________________________。
(3)D的结构简式为________________________________。
(4)由B生成C的化学方程式为______________________________________。
(5)芳香族化合物Y是D的同系物,Y的同分异构体能与饱和Na2CO3溶液反应放出气体,分子中只有1个侧链,核磁共振氢谱显示有5种不同化学环境的氢,峰值面积比为6:2:2:1:1。写出两种符合要求的Y的结构简式____________、________________________。
(6)写出以甲醛、丙醛和乙二醇为主要原料合成软质隐形眼镜高分子材料-聚甲基丙烯酸羟乙酯( )的合成路线(无机试剂自选):__________________________。
)的合成路线(无机试剂自选):__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com