
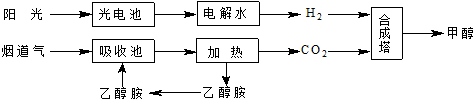
| ��Ӧʱ��/min | 3 | 5 | 7 | 10 | 13 |
| c��CO2��/mol•L-1 | 0.50 | 0.37 | 0.30 | 0.25 | 0.25 |
���� ��1���������ˮ����ƽ���е������ӣ��ٽ�ˮ����ƽ��������У�����������Ũ��������Һ�Լ��ԣ�
��2����2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��l������H1=-1451kJ/mol��
��2H2��g��+O2��g��=2H2O��l������H2=-571.6KJ/mol��
���ݸ�˹���ɣ�$\frac{3}{2}$����-�١�$\frac{1}{2}$�õ���ӦCO2��g��+3H2��g���TCH3OH��l��+H2O��l�������ø�˹���ɼ��㷴Ӧ�ȣ�����д�Ȼ�ѧ����ʽ��
��3����������ʽ�����K�ı���ʽ����ƽ�ⳣ����
��4���״��Ϳ���Ϊԭ�ϣ����ɼ���ȼ�ϵ�أ������ϼ״�ʧ��������̼������ӣ��������������õ��ӵĻ�ԭ��Ӧ���ݴ���д�缫��Ӧʽ��
��5�����ݻ��Ϸ�Ӧ���ص���������ƽ���ƶ�ԭ���жϷ�Ӧ�ķ���
��� �⣺��1���Ҵ���ˮ��Һ����������ȡ����������������ӣ�ʹ��Һ�е�����������Ũ������Ӧ�����ӷ���ʽΪ��HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-��
�ʴ�Ϊ��HOCH2CH2NH2+H2O?HOCH2CH2NH3++OH-��
��2���״���������ȼ������д���Ȼ�ѧ����ʽ�ֱ�Ϊ��
��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��l������H1=-1451kJ/mol��
��2H2��g��+O2��g��=2H2O��l������H2=-571.6KJ/mol��
���ݸ�˹���ɣ���ӦCO2��g��+3H2��g���TCH3OH��l��+H2O��l��
���Կ����Ƿ���ʽ$\frac{3}{2}$����-�١�$\frac{1}{2}$�����ԡ�H=��$\frac{3}{2}$��-571.6KJ/mol��-��-1451kJ/mol����$\frac{1}{2}$=-131.9KJ/mol��
�ʴ�Ϊ��CO2��g��+3H2��g���TCH3OH��l��+H2O��l����H=-131.9KJ/mol
��3��CO2��g��+3H2��g��?CH3OH��g��+H2O��g��
��ʼ��1mol/L 3mol/L 0 0
ת����0.75mol/L 2.25mol/L 0.75mol/L 0.75mol/L
ƽ�⣺0.25mol/L 0.75mol/L 0.75mol/L 0.75mol/L
��k=$\frac{0.75��0.75}{0.25��0.7{5}^{3}}$=5.3��
�ʴ�Ϊ��5.3��
��4���״��Ϳ���Ϊԭ�ϣ����ɼ���ȼ�ϵ�أ������ϼ״�ʧ��������̼������ӣ������ĵ缫��ӦʽΪ��2CH3OH-12e-+16OH-=2CO32-+12H2O�������������������õ��ӵĻ�ԭ��Ӧ������ӦΪ��O2+4e-+2H2O=4OH-��
�ʴ�Ϊ��O2+4e-+2H2O=4OH-��2CH3OH-12e-+16OH-=2CO32-+12H2O��
��5��������Ļ��Ϸ�Ӧ�Ƿ��ȵģ�����CO��g��+2H2��g��?CH3OH��g��Ϊ���ȷ�Ӧ�����Ѵ�ƽ��˷�Ӧ�ڱ�֤����Ũ�Ȳ��������£��������������������ֵ�Ũ�ȶ����䣬ѹǿ���䣬����ƽ�ⲻ���ƶ����ʴ�Ϊ�����ȣ�B��
���� ���⿼�����Ȼ�ѧ����ʽ��˹���ɵļ���Ӧ�ã���ѧƽ�ⳣ����Ӱ�������жϣ�ԭ��ء����صĵ缫��Ӧ��д��ԭ��Ӧ�ú͵����غ���㣬��Ŀ�Ѷ��е�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȼ�Լ���ǿ�����Լ��ֿ����ò�Զ���Դ | |
| B�� | ��ʪ��ĺ�ɫʯ����ֽ���鰱�� | |
| C�� | ��50ml��Ͳ������0.1000mol•L-1������ | |
| D�� | ʵ���Ҿƾ����Ż�ʱ����ʪĨ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1molH2O��������18g/mol | B�� | CO2��Ħ��������44g/mol | ||
| C�� | �����Ħ��������98g | D�� | HCl����Է���������36.5g/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͭ�ľ����У���ͭΪ���� | |
| B�� | ͭ�ڿ�����Ҳ�������⣬����ϡ����ϴ�� | |
| C�� | ͭ���������Խ�ǿ��������I-������Cu2+��S2-��Ӧ���������� | |
| D�� | ͭ�����Ա����������Cu2+������Ӧ����Fe3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������Ӧ�����ȼ����뱽�����ᷴӦ�����������ķ�Ӧ������ͬ | |
| B�� | ����ˮ���뱽�У���ˮ��ɫ����Ϊ�����˼ӳɷ�Ӧ | |
| C�� | ��֬�͵����ʶ����Է���ˮ�ⷴӦ | |
| D�� | �Ҵ�������������ɷ���ȡ����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
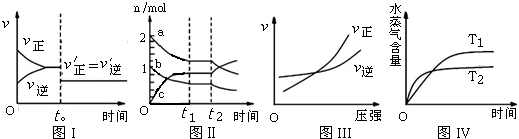
| A�� | ͼI����ӦH2+I2�T2HI ��ƽ���t0ʱ�����¶ȷ�Ӧ������ʱ��ı仯 | |
| B�� | ͼ��Ӧ2SO3�T2SO2+O2 ��ƽ��������������ʱ���ɷֵ����ʵ�����ʱ��ı仯��ͼ��a��b��c�ֱ����SO2��O2��SO3�����ʵ����ı仯���ߣ� | |
| C�� | ͼIII����ӦN2+3H2�T2NH3�ں�������£���Ӧ������ѹǿ�Ĺ�ϵ | |
| D�� | ͼIV����ӦCO2��g��+H2��g���TCO��g��+H2O��g����H��0��ˮ����������ʱ��ı仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �٢� | B�� | �٢� | C�� | �ڢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������Һ�а�ɫ�������ɣ�֤������������ | |
| B�� | �����Ȼ�����Һ�а�ɫ�������ɣ������ӹ�����ϡ���ᣬ��������ʧ��֤����Һ�к������������ | |
| C�� | ��Ũ����������Һ����ȣ�����ʹʪ���ɫʯ����ֽ���������壬֤������笠����� | |
| D�� | �������ᣬ�ų���ʹ����ʯ��ˮ����ǵ���ɫ��ζ���壬֤������̼������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʵ���ɫ��˵���������Ӷ����� | |
| B�� | ���ʵ��ۡ��е���˵���������Ӷ����� | |
| C�� | ������±�ص��ʴ���±�������û������Ŀ�������˵���������Ӷ����� | |
| D�� | ���ǵ��⻯����ȶ�����˵���������Ӷ���ǿ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com