
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
铁及其化合物与生产、生活关系密切。
(1)右图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。
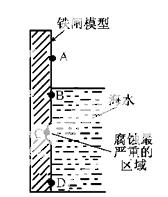
①该电化腐蚀称为 。
②图中A、B、C、D四个区域,生成铁锈最多的是 (填字母)。
(2)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:
 ①步骤I若温度过高,将导致硝酸分解。硝酸分解的化
①步骤I若温度过高,将导致硝酸分解。硝酸分解的化 学方程式为
学方程式为  。
。
②步骤II中发生反应:4Fe(NO3) 2+O2+(2n+4)H2O=2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为 。
2+O2+(2n+4)H2O=2Fe2O3·nH2O+8HNO3,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,该反应的化学方程式为 。
③上述生产流程中,能体现“绿色化学”思想的是 (任写一项)。
(3)已知t℃时,反应FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常数K=0.25。
Fe(s)+CO2(g)的平衡常数K=0.25。
①t℃时,反应达到平衡时n(CO):n(CO2)= 。
②若在1 L密闭容器中加入0.02 mol FeO(s),并通入xmolCO,t℃时反应达到平衡。此时FeO(s)转化率为50%,则x= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于①乙烯;②苯;③乙醇;④乙酸;⑤乙酸乙酯⑥硝基苯等有机物的叙述不正确的是
A.可以用NaOH溶液鉴别②③⑤⑥ B.①③能使酸性KMnO4溶液褪色
C.①④⑤都有双键,可与氢气加成 D.②③④⑤都能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如图1的装置:
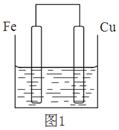 (以下均假设反应过程中溶液体积不变)。
(以下均假设反应过程中溶液体积不变)。
⑴铁片上的电极反应式为 。
⑵铜片周围溶液会出现 的现象。
⑶若2 min后测得铁片和铜片之间的质量差为1.2g,计算:
①导线中流过的电子的物质的量为 mo1;
②该段时间内用硫酸铜表示的平均反应速率为
查看答案和解析>>
科目:高中化学 来源: 题型:
下列条件下的X溶液均能跟少量盐酸反应,其中反应速率最快的是
A.10℃ 20 mL 3mol/L的X溶液 B.20℃ 30 mL 2mol/L的X溶液
C.20℃ 10 mL 4mol/L的X溶液 D.10℃ 10 mL 2mol/L的X溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列金属冶炼的反应原理,错误的是
A.2NaCl(熔融)  2Na+Cl2 B.MgO+H2
2Na+Cl2 B.MgO+H2 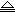 Mg+H2O
Mg+H2O
C.Fe3O4+4CO  3Fe+4CO2 D.2HgO
3Fe+4CO2 D.2HgO 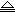 2Hg+O2
2Hg+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示的装置来制取乙酸乙酯。试回答下列问题:
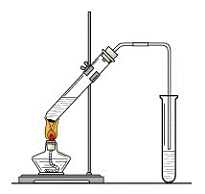 (1)写出由CH3COOH与C2H518OH制取乙酸乙酯的化学反应方程式 ;该反应属____反应。
(1)写出由CH3COOH与C2H518OH制取乙酸乙酯的化学反应方程式 ;该反应属____反应。
(2)该反应需加入一定量的浓硫酸,则浓硫酸的主要作用是 。
(3)右边试管内所盛饱和碳酸钠溶液的主要作用是
。
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 (填操作名称);主要使用的玻璃仪器是 。(答仪器的名称)
(6)生成乙酸乙酯的反应是可逆反应,反应物不能完全转化成生成物,反应一段时间后,达到了反应的限度,即达到化学平衡状态。下列描述能说明乙醇与乙酸的反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应速率与逆反应速率相等
⑤反应混合物中各物质的浓度不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com