
【题目】下列反应中既属于氧化还原反应,又属于吸热反应的是
A.灼热的碳与CO2反应B.Ba(OH)2·8H2O与NH4Cl反应
C.甲烷在氧气中燃烧D.铝片与稀硫酸反应
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:
【题目】海水提镁的主要流程如下,下列说法正确的是

①试剂M是盐酸 ②流程中的反应全部都是非氧化还原反应
③操作b只是过滤 ④用海水晒盐后的饱和溶液加石灰乳制Mg(OH)2
⑤采用电解法冶炼镁是因为镁很活泼
A. ①②③④⑤ B. ②③ C. ④⑤ D. ①④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.所有主族中都存在非金属元素
B.同周期元素中,第ⅦA族元素的原子半径最大
C.第ⅥA族元素的原子半径越大,越容易得到电子
D.元素周期表中第ⅢB族到第ⅡB族10个纵列的元素都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于吸热反应的是( )
A. C6H12O6(葡萄糖aq)+6O2![]() 6CO2+6H2O
6CO2+6H2O
B. 氢氧化钠溶液与盐酸的中和反应
C. 反应物的总能量大于生成物的总能量
D. 破坏反应物全部化学键所需能量大于破坏生成物全部化学键所需能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( ) 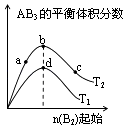
A.图中T2一定大于T1
B.图中b点速率一定大于d点速率
C.达到平衡时,A2的转化率大小为:c>b>a
D.加入催化剂可以使状态d变为状态b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】花椒毒素(Ⅰ)是白芷等中草药的药效成分,也可用多酚A为原料制备,合成路线如下:

回答下列问题:
(1)①的反应类型为_____________________;B分子中最多有_________个原子共平面。
(2)C中含氧官能团的名称为______________________;③的“条件a”为____________________。
(3)④为加成反应,化学方程式为__________________________________。
(4)⑤的化学方程式为__________________________________。
(5)芳香化合物J是D的同分异构体,符合下列条件的J的结构共有_________种,其中核磁共振氢谱为五组峰的J的结构简式为_________________。(只写一种即可)。
①苯环上只有3个取代基;②可与NaHCO3反应放出CO2;③1mol J可中和3mol NaOH。
(6)参照题图信息,写出以 为原料制备
为原料制备 的合成路线(无机试剂任选) :______________
的合成路线(无机试剂任选) :______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.2Al+Fe2O3![]() Al2O3+2Fe在化学反应过程中产生超高热,曾用于钢轨焊接。完成下列填空:
Al2O3+2Fe在化学反应过程中产生超高热,曾用于钢轨焊接。完成下列填空:
(1)氧元素在元素周期表中的位置为_______________,其离子结构示意图为__________。
(2)铝盐常用作净水剂,用文字和化学用语进行解释_______________________________。
(3)氧的非金属性强于氮,用元素周期律知识分析原因_____________________________。
(4)Al2O3与NaOH溶液反应的离子方程式为______________________________________。
II.NH4Al(SO4)2·12H2O水溶液呈_____性(选填“酸”、“碱”或“中”),比较溶液中离子浓度大小c(NH4+)_____c(Al3+)(选填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B3C+4D反应中,表示该反应速率最快的是( )
A.v(A)=0.5 mol/(Ls)
B.v(B)=0.3 mol/(Ls)
C.v(C)=0.8 mol/(Ls)
D.v(D)=1 mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组研究溶液中Fe2+与NO2、NO3的反应。资料: [Fe(NO)]2+在溶液中呈棕色。

(1)研究现象a中的黄色溶液。
①用______溶液检出溶液中含有Fe3+。
②甲认为是O2氧化了溶液中的Fe2+。乙认为O2不是主要原因,理由是______。
③进行实验Ⅱ,装置如图。左侧烧杯中的溶液只变为黄色,不变为棕色,右侧电极上产生无色气泡,经检验该气体为NO。

产生NO的电极反应式是______。
实验Ⅱ的目的是______。
(2)研究现象a中的棕色溶液。
①综合实验Ⅰ和实验Ⅱ,提出假设:现象a中溶液变为棕色可能是NO与溶液中的Fe2+或Fe3+发生了反应。进行实验Ⅲ,证实溶液呈棕色只是因为Fe2+与NO发生了反应。实验Ⅲ的操作和现象是______。
②加热实验Ⅰ中的棕色溶液,有气体逸出,该气体在接近试管口处变为红棕色,溶液中有红褐色沉淀生成。解释产生红褐色沉淀的原因是______。
(3)研究酸性条件下,溶液中Fe2+与NO2、NO3的反应。
序号 | 操作 | 现象 |
ⅰ | 取1 mol·L1的NaNO2溶液,加醋酸至pH=3,加入1 mol·L1FeSO4溶液 | 溶液立即变为棕色 |
ⅱ | 取1 mol·L1的NaNO3溶液,加醋酸至pH=3,加入1 mol·L1FeSO4溶液 | 无明显变化 |
ⅲ | 分别取0.5 mL 1 mol·L1的NaNO3溶液与1 mol·L1的FeSO4溶液,混合,小心加入0.5 mL浓硫酸 | 液体分为两层,稍后,在两层液体界面上出现棕色环 |
①ⅰ中溶液变为棕色的离子方程式是______、______。
②ⅲ中出现棕色的原因是______。
实验结论:本实验条件下,溶液中NO2、NO3的氧化性与溶液的酸碱性等有关。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com