
在下列各溶液中,离子一定能大量共存的是
A.强碱性溶液中: 、
、 、
、 、
、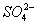
B.室温下, 的盐酸中:
的盐酸中: 、
、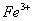 、
、 、
、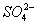
C.含有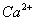 的溶液中:
的溶液中: 、
、 、
、 、
、
D.由水电离产生的 的溶液中:
的溶液中: 、
、 、
、 、
、
科目:高中化学 来源: 题型:
在用浓硫酸配制稀硫酸过程中,下列实验操作对所配制的稀硫酸的物质的量浓度有何影响?(在后面横线上“偏高”、“偏低”、“无影响”)。(4分)
I、用量筒量取浓硫酸时俯视凹液面
II、定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
Ⅲ、定容时仰视刻度线
Ⅳ、转移时容量瓶中有少量蒸馏水
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释事实的反应方程式不正确的是
A.氨水使酚酞溶液变红:


B.醋酸使碳酸钙溶解: 
C.草酸溶液使高锰酸钾酸性溶液褪色: 
D.向污水中投放明矾,生成能凝聚悬浮物的胶体: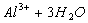


查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是
A.用惰性电极电解 溶液分别得到单质
溶液分别得到单质 和Cl2
和Cl2
B.常温下,某溶液中由水电离出的 ,该溶液一定呈酸性
,该溶液一定呈酸性
C. 溶液和
溶液和 溶液加热蒸干、灼烧都得到
溶液加热蒸干、灼烧都得到
D.在AgBr饱和溶液中加入AgNO3溶液,达到平衡时,溶液中Br-浓度降低
查看答案和解析>>
科目:高中化学 来源: 题型:
I:常温下,将某一元酸HA和NaOH溶液等体积混合,分别进行编号为①、②、③的实验,实验数据记录如下表
| 序号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
请回答:(1)根据①组实验情况,分析混合溶液的pH=9的原因是______________ ___。
(用反应的离子方程式表示),在该溶液中下列关系式不正确的是(填序号字母)________。
A.c(Na+)+c(H+)=c(OH-)+c(A-) B.c(Na+)=c(HA)+c(A-)
C.c(HA)+c(H+)=c(OH-) D.c(Na+)+c(H+)=c(OH-)+c(A-)+c(HA)
(2)②组情况表明,c __0.2mol·L-1(选填“>”、“<”或“=”)。混合溶液中离子浓度c(A-)________c(Na+)(选填“>”、“<”或“=”)
从③组实验结果分析,说明HA的电离程度________NaA的水解程度(选填“>”、“<”或“=”),离子浓度由大到小的顺序是______________________________________。
Ⅱ:室温下,若将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示。
(1)NH3·H2O的电离方程式是 。
(2)b点所示溶液中的溶质是 。
(3)c点所示溶液中,离子浓度从大到小的关系为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体),向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示,下列分析或结果错误的是
 A.H2SO4浓度为4mol•L—1
A.H2SO4浓度为4mol•L—1
B.OA段产生的是NO,AB段的反应为
Fe+2Fe3+=3Fe2+,BC段产生氢气
C.每份混合酸中NO3—物质的量为0.3mol
D.第二份溶液中最终溶质为FeSO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com