
 在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:2SO2(g)+O2(g)═2SO3(g)△H=-190kJ•mol-1
在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:2SO2(g)+O2(g)═2SO3(g)△H=-190kJ•mol-1分析 (1)化学反应2SO2(g)+O2(g)?2SO3(g)△H=-190kJ•mol-1是放热反应,升温,平衡逆向进行,平衡常数减小;
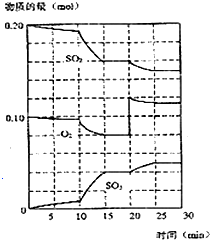
(2)反应混合物各物质的物质的量不变化,说明反应处于平衡状态;
(3)由图可知,反应进行至20min时,平衡向正反应移动,瞬间只有氧气的浓度增大;由图可知,反应向正反应进行,10min到15min反应混合物单位时间内的变化量增大,说明反应速率增大,10min改变瞬间,各物质的物质的量不变.据此结合选项分析;
(4)提高二氧化硫转化率,平衡正向进行,依据平衡移动原理分析判断;
解答 解:(1)2SO2(g)+O2(g)?2SO3(g)△H=-190kJ•mol-1,反应是放热反应,升温平衡逆向进行,平衡常数减小,所以该反应500℃时的平衡常数小于该反应400℃时的平衡常数,故答案为:<;
(2)反应混合物各物质的物质的量不变化,说明反应处于平衡状态,由图可知在15-20min和25~30 min出现平台,各组分的物质的量不变,反应处于平衡状态,
故答案为:15-20min和25~30 min;
(3)由图可知,反应进行至20min时,平衡向正反应移动,瞬间只有氧气的浓度增大,应是增大O2浓度(通入O2);
由图可知,反应向正反应进行,10min到15min反应混合物单位时间内的变化量增大,说明反应速率增大,10min改变瞬间,各物质的物质的量不变.
A.加了催化剂,增大反应速率,故A正确;
B.缩小容器体积,增大压强,增大反应速率,故B正确;
C.降低温度反应速率降低,故C错误;
D.10min改变瞬间,各物质的物质的量不变,不是增加SO3的物质的量,故D错误;
故答案为:增大O2浓度(通入O2);AB;
(4)欲提高SO2的转化率,平衡正向进行,
a.向装置中再充入N2,恒温恒容容器,总压增大,分压不变,平衡不动,故a不符合;
b.两种反应物增加一种会提高另一种的转化率,向装置中再充入O2,二氧化硫转化率增大,故b符合;
c.改变反应的催化剂,改变反应速率但不改变化学平衡,故二氧化硫转化率不变,故c不符合;
d.反应是放热反应,升高温度平衡逆向进行,二氧化硫转化率减小,故d不符合;
故答案为:b;
点评 本题考查了化学平衡的特征、化学平衡的判断、平衡常数的概念、计算应用,图象分析和数据应用能力,化学平衡状态的判断是高考的热点,注意化学平衡常数只与温度有关,与其他物理量无关,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 鉴别胶体与浊液(丁达尔效应) | B. | 高压除尘(电泳现象) | ||
| C. | 河海交汇处可沉积沙洲(聚沉) | D. | 喷雾剂的应用(布朗运动) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
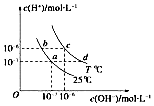
| A. | 若从a点到c点,可采用在水中加入酸的方法 | |
| B. | b点对应的醋酸中由水电离的c(H+)=10-6mol•L-1 | |
| C. | T℃时,0.05 mol•L-1的Ba(OH)2溶液的pH=11 | |
| D. | c点对应溶液的Kw大于d点对应溶液的Kw |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
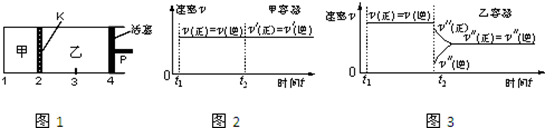
| A. | 保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加 | |
| C. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 | |
| D. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①④③② | C. | ④①②③ | D. | ④③②① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其他分散系的本质特征是胶体具有丁达尔现象 | |
| B. | NaCl溶液在电流的作用下电离成Na+与Cl- | |
| C. | 2NO2+2NaOH═NaNO3+NaNO2+H2O是氧化还原反应 | |
| D. | 固体NaCl不导电,所以NaCl是非电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com