
【题目】

(1)该硫酸的物质的量浓度是________mol/L。
(2)某化学兴趣小组进行硫酸性质的实验探究时,需要490 mL 4.6 mol/L的稀硫酸,则需要取________mL的该硫酸。
(3)配制时,所需的玻璃仪器除量筒、烧杯、玻璃棒和胶头滴管之外,还需要 (填仪器名称);
(4)配制溶液有如下(未按顺序排列):a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,f.将溶液移至容量瓶,g.定容等操作。其中摇匀的前一步操作是 ;(填写字母)
(5)在下列配制过程示意图中,有错误的是(填写序号) 。
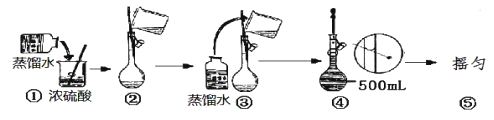
(6)在配制4.6 mol/L的稀硫酸的过程中,下列情况会引起硫酸溶液物质的量浓度偏高的是
A.未经冷却趁热将溶液注入容量瓶中 | B.容量瓶洗涤后,未经干燥处理 |
C.定容时仰视观察液面 | D.未洗涤烧杯和玻璃棒 |
【答案】(1)18.4(2)125(3)500ml容量瓶(4)g(5)14(6)A
【解析】试题分析:(1)该硫酸的物质的量浓度是![]() =18.4mol/L;(2)根据稀释前后溶质物质的量相同,
=18.4mol/L;(2)根据稀释前后溶质物质的量相同,![]() ,v=0.125L,则需要取125mL的该硫酸;(3)配制时,所需的玻璃仪器除量筒、烧杯、玻璃棒和胶头滴管之外,还需要500ml容量瓶;(4)摇匀的前一步操作是定容操作;(5)不能把水倒入浓硫酸中;定容时视线要平视刻度线;(6)未经冷却趁热将溶液注入容量瓶中,溶液体积偏小,浓度偏大;容量瓶洗涤后,未经干燥处理,无影响;定容时仰视观察液面,溶液体积偏大,浓度偏小;未洗涤烧杯和玻璃棒,溶质偏少,浓度偏小。
,v=0.125L,则需要取125mL的该硫酸;(3)配制时,所需的玻璃仪器除量筒、烧杯、玻璃棒和胶头滴管之外,还需要500ml容量瓶;(4)摇匀的前一步操作是定容操作;(5)不能把水倒入浓硫酸中;定容时视线要平视刻度线;(6)未经冷却趁热将溶液注入容量瓶中,溶液体积偏小,浓度偏大;容量瓶洗涤后,未经干燥处理,无影响;定容时仰视观察液面,溶液体积偏大,浓度偏小;未洗涤烧杯和玻璃棒,溶质偏少,浓度偏小。


科目:高中化学 来源: 题型:
【题目】中国自古有“信口雌黄”、“雄黄入药”之说。雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。根据题意完成下列填空:
(1) 砷元素有+2、+3两种常见价态。As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体,写出该反应的化学方程式_____________________。
(2) 上述反应中的氧化剂是___________;氧化产物是___________;反应产生的H2S气体可用____________吸收。
(3)As2S3和HNO3有如下反应:As2S3+10H++ 10NO3—=2H3AsO4+3S+10NO2↑+ 2H2O。若生成1mol H3AsO4,则反应中转移电子的物质的量为___________;若将该反应设计成一原电池,则NO2应该在___________(填“正极”或“负极”)附近逸出。
(4)若反应产物NO2与11.2LO2(标准状况)混合后用水吸收全部转化成浓HNO3,然后与过量的碳反应,写出碳与浓硝酸反应的化学方程式__________________;所产生的CO2的量___________(选填编号)。
A.小于0.5mol B.等于0.5mol C.大于0.5mol D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冬季的降雪给机场和马路带来诸多不便,其中醋酸钾(CH3COOK)是融雪效果较好的融雪剂,下列关于醋酸钾说法正确的是
A. 1 mol CH3COOK的质量为98 g·mol-1
B. CH3COOK的摩尔质量等于它的相对分子质量
C. 一个CH3COOK微粒的质量约为![]() g
g
D. 含有6.02×1023个碳原子的CH3COOK的物质的量为1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醛在有机合成中十分重要,已知如下反应:
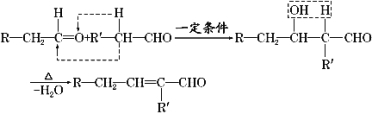
由枯茗醛合成兔耳草醛的传统合成路线如图所示:
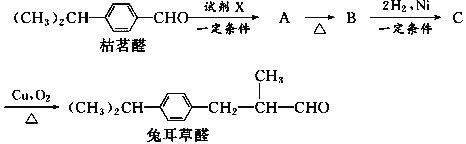
(1)写出试剂X的结构简式:__________________。
(2)写出有机物B的结构简式:__________________________。
(3)写出有机物C →兔耳草醛的化学方程式:________________________。
(4)人们最新研究的兔耳草醛的合成路线,该路线原子利用率理论上可达100%:

试写出D的结构简式:_________________________。
(5)芳香族化合物Y与枯茗醛互为同分异构体,Y具有如下特征:
a.不能发生银镜反应,可发生消去反应;
b.核磁共振氢谱显示:Y消去反应产物的环上只存在一种化学环境的氢原子。写出Y所有可能的结构简式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.聚合物( )可由单体CH3CH=CH2和CH2=CH2加聚制得
)可由单体CH3CH=CH2和CH2=CH2加聚制得
B.在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应
C.油脂皂化反应得到高级脂肪酸盐与甘油
D.己烷有4种同分异构体,它们的熔点、沸点各不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池和电解池的比较中正确的是
A.能量转化形式相同
B.两极的名称相同
C.负极和阴极上移向的离子类别相同
D.负极和阳极上发生的反应类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A原子核中无中子且A和C同主族,A和B形成的化合物在水中呈碱性,单质D在单质E中可燃烧产生白色烟雾。回答下列问题:
(1)除B外,上述元素的电负性从大到小依次为 ;(用元素符号表示)
(2)B的氢化物与同主族第三、第四周期所形成的氢化物沸点由高到低的排列顺序是 (用化学式表示),原因是 ;
(3)A和D形成的化合物的中心原子的杂化类型为 ;A和B形成的化合物BA5中存在的化学键类型为 ;
(4)单质D的一种含氧酸可表示为H3DO3,它是二元弱酸,请写出它与足量的氢氧化钠溶液反应的离子方程式____________;
(5)C 的一种氧化物的晶胞结构如图所示,晶胞参数a=0.566 nm,晶胞中C原子的配位数为 ;此晶体的密度(g·cm-3)为 (只列式不计算)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z 为不同短周期非金属元素的气态单质。在一定条件下能发生如下反应:
Y+X→甲(g),Y+Z→乙(g)。甲为10电子分子,Z为黄绿色气体。甲、乙可化合生成离子化合物。
(1)X 的电子式是______________。
(2)写出Y+X→甲(g)的化学方程式_____________________。
(3)向一定浓度的 BaCl2溶液中通入 SO2气体,未见沉淀生成,若在通入 SO2气体的同时加入或通入某纯净物(从X、Y、Z、甲、乙中选择),即可生成白色沉淀,该纯净物的化学式为________,生成的白色沉淀的化学式为___________。
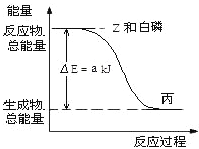
(4)已知常温下,PCl3为液体,PCl5为固体。白磷(P4)在Z气体中燃烧生成液态丙分子,白磷固体和 Z 气体反应,生成1 mol液态丙时,能量变化如图所示,写出该反应的热化学方程式_______________。
已知1 mol白磷固体和Z气体反应,生成固态丁时,放热b kJ,则1 mol固态丁转化为液态丙时的反应热ΔH=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】γ-Fe2O3在磁性、催化、气敏等方面用途非常广泛,以硫铁矿烧渣(含Fe2O3、SiO2、CaO、Al2O3等)为原料生产γ-Fe2O3的流程如下:

(1)“还原焙烧”时,焦炭的作用是______________,起还原作用的主要物质是__________(填化学式)。
(2)“浸取”时,为提高铁的浸取率,可采取的措施除粉碎焙烧后的熔体、适当增大硫酸的用量外,还可采取的措施有______________(任写一条)。
(3)“过滤”前,将溶液的pH调至5~5.5的目的是将Al3+转化为___________(填化学式)。
(4)“缓慢干燥”生成铁黄的化学方程式为_____________。
(5)经上述流程制得的γ-Fe2O3中含有少量FeO和Al2O3杂质,某课题小组称取8.1380gγ-Fe2O3样品,溶于100mL2.00mol/LH2SO4溶液中,完全溶解后加入过量H2O2溶液,然后加入1.00mol/L的NaOH溶液,生成固体的质量与加入NaOH溶液体积的关系如图,则该样品中γ-Fe2O3的百分含量为___________(百分数保留到小数点后两位)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com