

| A、此一元弱酸的电离常数(Ka)约为1.0×10-6 |
| B、此弱酸的浓度为1×10-4mol/L |
| C、此实验最好选用甲基红(变色范围在4.2~6.3)作指示剂 |
| D、此滴定反应为吸热反应 |
| 10-4×10-4 |
| 10-2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
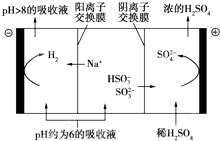 最近雾霾天气又开始肆虐我国大部分地区.其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2.
最近雾霾天气又开始肆虐我国大部分地区.其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2.| n(SO32-):n(HSO3- ) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2(g)+I2(g)?2 HI(g) |
| B、3H2(g)+N2(g)?2NH3(g) |
| C、2SO2(g)+O2(g)?2SO3(g) |
| D、C(s)+CO2(g)?2CO(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:
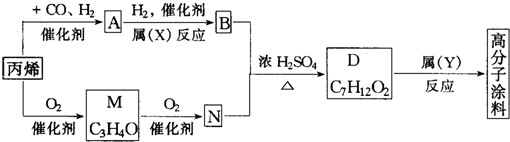
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
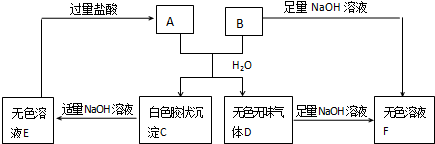
查看答案和解析>>
科目:高中化学 来源: 题型:
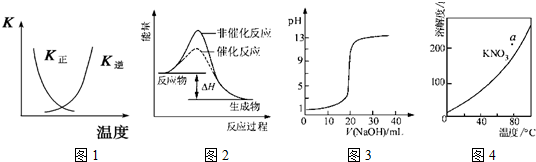
| A、图1表示该可逆反应平衡后,随温度升高,平衡会逆向移动 |
| B、图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| C、图3表示0.1000mol?L-1NaOH溶液滴定20.00mL0.1000mol?L-1醋酸溶液所得到的滴定曲线 |
| D、图4表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的过饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molH2SO4与1molBa(OH)2完全中和所放出的热量为中和热 |
| B、中和反应都是放热反应 |
| C、氢气燃烧放出大量的热,说明参加反应的氢气和氧气总能量比生成物水的总能量高 |
| D、CO燃烧是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com