
按图的装置进行电解,A极是铜锌含金,B极为纯铜.电解质溶液中含有足量的Cu2+.通电一段时间后,若A极恰好全部溶解,此时B极质量增加7.68g,溶液质量增加0.03g,则A极合金中Cu、Zn的原子个数比为()
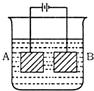
A. 4:1 B. 3:1 C. 2:1 D. 5:3
考点: 电解原理.
专题: 电化学专题.
分析: 该装置是电解池,阳极上金属失电子发生氧化反应,阴极上铜离子得电子发生还原反应,所以阴极上增加的质量是铜的质量,溶液中增加的质量为溶解锌的质量与通过相同电子时析出铜的质量差,根据质量差可以计算溶解的锌的物质的量,再根据氧化还原反应中得失电子数相等计算合金上铜的物质的量,从而计算铜和锌的原子个数之比.
解答: 解:B极上析出的是铜,B极质量增加7.68g,其物质的量=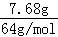 =0.12mol;
=0.12mol;
阳极上溶解锌时,阴极上析出铜,所以溶液质量增加的质量为锌和铜的质量差,溶液质量增加0.03g,即锌和铜的质量差为0.03g.
设锌的物质的量为x.
Zn+Cu2+=Zn2++Cu 质量增加
1mol 1g
x 0.03g
x=0.03mol.
即合金中锌的物质的量是0.03mol.
根据氧化还原反应中得失电子数相等知,阳极上锌和铜失去的电子数等于阴极上铜离子得到的电子,设铜的物质的量为y.
0.03mol×2+2y=0.12mol×2
y=0.09mol,
所以铜和锌的物质的量之比为0.09mol:0.03mol=3: 1,所以铜和锌的原子个数之比是3:1,
故选:B.
点评: 本题以原电池原理为载体考查了物质的量的有关计算,明确溶液中质量增加的量是什么是解本题的关键,然后根据得失电子数相等计算铜的物质的量,从而确定铜和锌的个数之比.


 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
常温下体积相同的下列四种溶液:①pH=3的盐酸②pH=3的醋酸溶液③pH=11的氨水④pH=11的NaOH溶液.下列说法中,正确的是()
A. ②和④混合,所得混合溶液的pH大于7
B. 将四种溶液分别稀释到体积为原的100倍,溶液pH大小顺序③>④>②>①
C. ③和④分别与足量稀硫酸中和,消耗硫酸的体积③=④
D. ①和③混合,所得混合溶液中c(H+)+c(NH4+)=c(Cl﹣)+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
在100g碳不完全燃烧所得气体中,CO占1/3体积,CO2占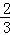 体积,且:
体积,且:
C(s)+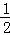 O2(g)═CO(g)△H=﹣110.35kJ;
O2(g)═CO(g)△H=﹣110.35kJ;
CO(g)+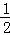 O2(g)═CO2(g)△H=﹣282.5kJ
O2(g)═CO2(g)△H=﹣282.5kJ
与这些碳完全燃烧相比,损失的热量是()
A. 392.92 kJ B. 2489.4 kJ C. 784.72 kJ D. 3274.3 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
若在铜片上镀银时,下列叙述正确的是()
①将铜片接在电源的正极上
②将银片接在电源的正极上
③在铜片上发生的反应是:Ag++e﹣→Ag
④在银片上发生的反应是:4OH﹣﹣4e﹣→O2↑+2H2O
⑤需用硫酸铜溶液为电镀液
⑥需用硝酸银溶液为电镀液.
A. ①③⑥ B. ②③⑥ C. ①④⑤ D. ②③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
在水中加入等物质的量的Ag+、Pb2+、Na+、SO42﹣、NO3﹣、Cl﹣,该溶液放在用惰性材料做电极的电解槽中,通电片刻后,则氧化产物与还原产物的质量之比为()
A. 35.5:108 B. 16:207 C. 8:1 D. 108:35.5
查看答案和解析>>
科目:高中化学 来源: 题型:
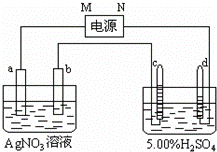
图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体.回答:
(1)直流电源中,M为 极.
(2)Pt电极上生成的物质是银,其质量为 g.
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为:2: : :1.
(4)AgNO3溶液的浓度(填增大、减小或不变.下同) ,AgNO3溶液的pH ,H2SO4溶液的浓度 ,H2SO4溶液的pH .
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液的质量为 g.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是
A. 等物质的量的NaX和弱酸HX混合后的溶液中c(HX)可能大于c(X-)
B. 在pH=4.5的NaHSO3溶液中,c(H2SO3)大于c(SO32-)
C. 向0.1 mol/L醋酸溶液中加水稀释的过程中c(OH-)不断增大
D. 向含有Na2SO4的BaSO4悬浊液中加水稀释,c(Ba2+)增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com