
���й���ʮ���ֻ�ѧ���ţ�
��O2 ��614C ��238U ��1123Na ��O3 ��714N ��1224Mg ��
��235U ��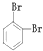 ��11��
��11�� ��12��
��12��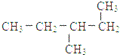
����
��1����ʾ���صķ��Ź��Уߣߣ���.
��2����Ϊͬλ�ص��ǣߣߣߣ�����ţ�������ͬ��.
��3����������ȣ������ܻ���ͬλ�ص��ǣߣߣ�.
��4����������ȣ�������������ȵ��ǣߣߣ�.
��5����Ϊͬ����������ǣߣߣ�.
��6����Ϊͬ���칹����ǣߣߣߣ�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ȼ������Ȼ����ˮ������γɵľ������ʣ���Ҫ�����ڶ�����ͺ��״�½���С��ݲⶨÿ0.1m3���塰��ȼ����Ҫ�ͷ�20��3�ļ������壬������˵���в���ȷ���� �� ��
A����ȼ���ͷŵļ������������� B����ȼ����ˮ���ͣ����ڻ�ѧ�仯
C����ȼ������Ϊ����ĺ�����Դ��D����ظ�ԭ���ܴ��ھ�����Ŀ�ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��.��8�֣��ºϳɵ�һ��������̼�ܳ��������壨��ͼ��ʾ��
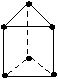 ��1��д�������ķ���ʽ
��1��д�������ķ���ʽ
��2��������һ��ȡ�����Ƿ���ͬ���칹��
��3�������Ķ���ȡ�����ж�����
��4��������ͬ���칹���ж��֣�����1�ֲ���ʹ���Ը��������Һ��Br2-CCl4��Һ��ɫ������һ���������ܸ��壨��H2������ȡ������ӳɣ���Ӧ������ͬ���칹��Ľṹ��ʽ�� ��
��.��6�֣�����ϩΪԭ�Ϻϳɻ�����C������������ʾ��

��1��д��A�Ľṹ��ʽ ��д���Ҵ��ĵ���ʽ
��2����Ӧ�٢ܵķ�Ӧ���ͷֱ�Ϊ �� ��
��3��д����Ӧ�ںܵ͢Ļ�ѧ����ʽ��
�� ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���淴ӦH2(g) �� I2(g)  2HI(g)�ﵽƽ��ı�־�� �� ��
2HI(g)�ﵽƽ��ı�־�� �� ��
A��H2��I2��HI��Ũ����� B��H2��I2��HI��Ũ�ȱ��ֲ���
C�����������ܶȱ��ֲ��� D�����������������ٸı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�屽��һ�ֳ��õĻ���ԭ�ϡ�ʵ�����Ʊ��屽
��ʵ�鲽�����£�
����1����a�м���15 mL����������м���ٽ�b��4.0 mL
Һ���������뵽a�У���ַ�Ӧ��
����2����a�м���10 mLˮ��Ȼ����˳�ȥδ��Ӧ����м��
����3����Һ������10 mLˮ��8 mL 10%��NaOH��Һ��10 mL ˮϴ�ӣ���Һ�ô��屽��
 ����4����ֳ��Ĵ��屽�м�����������ˮ�Ȼ��ƣ����á����˼��ôֲ�Ʒ��
����4����ֳ��Ĵ��屽�м�����������ˮ�Ȼ��ƣ����á����˼��ôֲ�Ʒ��
| �� | �� | �屽 | |
| �ܶ�/g��cm��3 | 0.88 | 3.10 | 1.50 |
| �е�/�� | 80 | 59 | 156 |
| ��ˮ�е��ܽ�� | �� | �� | �� |
(1)����d�������� ��
(2)��b�е�Һ���������뵽a�У������ܿ��ټ����ԭ���� ��
(3)����c��������������������������Ҫ������ (�ѧʽ)��
(4)����4�õ��Ĵֲ�Ʒ�л��������ʱ�����֪�����屽���й������������ϱ�����Ҫ��һ���ᴿ�ֲ�Ʒ����������е�ʵ����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��ȷ���ǣ� ��
A����ʯī���缫���CuSO4��Һ�� 2Cu2++2H2O 2Cu+O2��+4H+
2Cu+O2��+4H+
B������þ��Һ������������Һ��ϣ� SO42- + Ba2+ = BaSO4��
C��Cl2ͨ��ˮ�У� Cl2+H2O=2H+ +Cl-+ClO-
D��AlCl3��Һ�м��������ˮ�� Al3++4NH3•H2O = AlO2-+ 4NH4+ +2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�±�ΪԪ�����ڱ���һ���֣������Ԫ�آ١����ڱ��е�λ�ã��û�ѧ����ش��������⣺





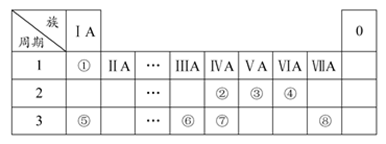
(1) �ڢۢߵ���ۺ����������������ǿ��˳����(�û�ѧʽ��ʾ) ��
(2) д���ɢܢ�����Ԫ����ɵļȺ����Ӽ����ֺ��Ǽ��Թ��ۼ��Ļ�����ĵ���ʽ ��
(3) �١�������Ԫ�ذ�ԭ�Ӹ���֮��Ϊ1��1��ɵij���Һ̬�������������Һ���ܽ�
Fe2��������д���÷�Ӧ�����ӷ���ʽ ��
(4) �٢ۢ�����һ�ֻ������ԭ�Ӹ���֮��Ϊ4�U1�U1���û�����Ļ�ѧʽΪ_________���û������ˮ��Һ�����ԣ������ӷ���ʽ��ʾ�������Ե�ԭ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������������������Ժ��ֱ�����ϣ�ֻҪ������һ������ȫȼ�ղ�����H2O������Ҳһ������ ��HCHO ��HCOOCH3 �� CO(NH2)2 ��C7H6
A���� B���٢� C���٢ڢ� D���٢ڢۢ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com