
| Ԫ�ش��� | A | B | C | D | E |
| ԭ�Ӱ뾶/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +6��-2 | -1 | -2 |
���� ������Ԫ���У�C��E����-2�ۣ����ڢ�A�壬C��+6����ԭ�Ӱ뾶C��E����CΪ��EΪ����D��-1�ۣ�ԭ�Ӱ뾶����������DΪCl��A��B���ϼ۷ֱ�Ϊ+2��+3���ֱ��ڢ�A�塢��A�壬ԭ�Ӱ뾶A��B����AΪMg��BΪAl���Դ˽����⣮
��� �⣺������Ԫ���У�C��E����-2�ۣ����ڢ�A�壬C��+6����ԭ�Ӱ뾶C��E����CΪ��EΪ����D��-1�ۣ�ԭ�Ӱ뾶����������DΪCl��A��B���ϼ۷ֱ�Ϊ+2��+3���ֱ��ڢ�A�塢��A�壬ԭ�Ӱ뾶A��B����AΪMg��BΪAl��
��1��CΪ��Ӧ���⻯�ﺬ��2��S-H�����ṹʽΪH-S-H���ʴ�Ϊ��H-S-H��
��2��B������������ˮ����ΪAl��OH��3��C������������ˮ����ΪH2SO4�����߷�Ӧ�����ӷ���ʽΪ��Al��OH��3+3H+=Al3+3H2O��
�ʴ�Ϊ��Al��OH��3+3H+=Al3+3H2O��
��3����������Ԫ����Cl�ķǽ�������ǿ��������������Ӧˮ�����������ǿ���� HClO4���ʴ�Ϊ��HClO4��
��4��C��E�γɵĻ�������SO2��SO3���ʴ�Ϊ��SO2��SO3��
��5��A��D���γɻ�����ΪMgCl2���������Ӿ��壬�ʴ�Ϊ�����Ӿ��壮
���� ���⿼��ṹ����λ�ù�ϵ�ۺ�Ӧ�ã�Ϊ�߿��������ͣ�������ѧ���ķ��������Ŀ��飬����ԭ�Ӱ뾶�뻯�ϼ��ƶ�Ԫ���ǽ���ؼ���ע���Ԫ�������ɵ��������գ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol Na���Ҵ���ȫ��Ӧ��ʧȥ2NA���� | |
| B�� | ��״���£�22.4L����NA��C6H6���� | |
| C�� | 0.5mol-OH��0.5mol OH-������5NA���� | |
| D�� | ���³�ѹ��8gCH4��5NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��3-����ϩ�ķ���ʽ��C4H6 | B�� | ������ĵ���ʽ��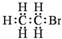 | ||
| C�� | ��ȩ�Ľṹʽ��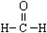 | D�� | �����ǵĽṹ��ʽ��CH2OH��CHOH��4CHO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�µ�33.6L������27g����ַ�Ӧ��ת�Ƶ�����Ϊ3NA | |
| B�� | ��״���£�22.4LNO��11.2L������ϣ�����ķ�������Ϊ1.5 NA | |
| C�� | 7.8 g Na2O2���е���������ĿΪ0.1 NA | |
| D�� | 80mL10mol/L��Ũ����������MnO2��Ӧ��ת�Ƶ�����Ϊ0.4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol18O2����������Ϊ16NA | |
| B�� | 100mL pH=3�Ĵ�����Һ�У���������ĿС��10-4NA | |
| C�� | 0.5mol���ֱ��������ռ�����ᷴӦת�Ƶĵ�������ȣ���Ϊ1.5NA | |
| D�� | ��״���£�11.2L SO3����������Ϊ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������顢���Ȼ�̼ | B�� | �����������Ҵ������Ȼ�̼ | ||
| C�� | �屽���Ҵ������Ȼ�̼ | D�� | �屽���Ҵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
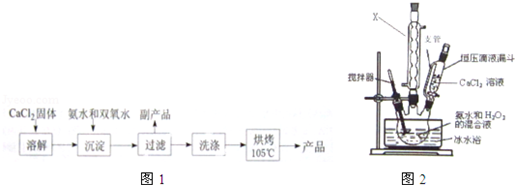
| ʵ����� | ��1�� | ��2�� | ��3�� | ��4�� |
| ����KMnO4���/mL | 19.98 | 20.02 | 20.20 | 20.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
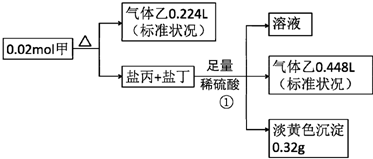
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
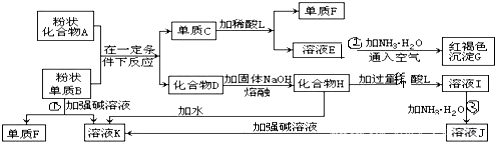
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com