
下列有关化学用语错误的是
A.碳酸的二级电离方程式:H2O+HCO3- H3O++CO32-
H3O++CO32-
B.玉的化学成分多为含水钙镁硅酸盐,如:Ca2Mg5Si8O22(OH)2可用氧化物表示为2CaO·5MgO·8SiO2·H2O
C.NaH与重水反应的方程式:NaH+D2O=NaOD+HD↑
D.均含有NA个电子的H2O和CH4具有相同的体积
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源:2016届福建省高三上学期半期考试化学试卷(解析版) 题型:推断题
A~G各物质间的关系如图,其中B、D为气态单质。
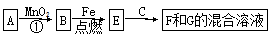
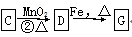
请回答下列问题:
(1)物质C、E分别为 、 。(填名称)
(2)反应①可选用不同的A进行,若反应在常温下进行,其化学方程式为 。
(3)请设计实验检验F、G的混合溶液中F的金属阳离子。(写出试剂、操作、现象、结论) 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上期中测试化学试卷(解析版) 题型:选择题
除去下列物质中的杂质(括号内为杂质),所选用的试剂及操作方法均正确的一组是
选项 | 混合物 | 选用的试剂 | 操作的方法 |
A | CaO(CaCO3) | 水 | 溶解、过滤、结晶 |
B | Cu(CuO) | 稀盐酸 | 溶解、过滤、洗涤、干燥 |
C | CuSO4(H2SO4) | 氢氧化钠溶液 | 过滤 |
D | CO(H2) | 氧气 | 点燃 |
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
设NA 代表阿伏加德罗常数的数值,下列说法正确的是
A.标准状况下,44.8 L NO与22.4 LO2混合后气体中分子总数为3NA
B.标准状况下,NA个SO3分子所占的体积约为22.4 L
C.标准状况下,22. 4L氯气与足量氢氧化钠溶液反应转移的电子数为NA
D.将0.1mol氯化铁溶于水配成1L溶液,所得溶液含有0.1NA Fe3+
查看答案和解析>>
科目:高中化学 来源:2016届浙江省嘉兴市高三上学期期中测试化学试卷(解析版) 题型:实验题
络氨铜【[Cu(NH3)4]SO4】是一种重要的染料及农药中间体。已知:①以氧化铜为主要原料合成该物质的合成路线如下图:
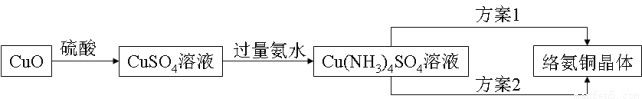
②络氨铜在乙醇-水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如下。
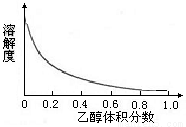
③(NH4)2SO4在水中可溶,在乙醇中难溶。
请根据以上信息回答下列问题:
(1)由CuO制出的CuSO4溶液中常含有 Fe2(SO4)3杂质,请设计一个可行方案,检验CuSO4溶液中是否含有Fe3+: 。
(2)[Cu(NH3)4]SO4 在水中存在如下解离过程:[Cu(NH3)4]SO4===[Cu(NH3)4]2+(深蓝色离子)+SO42-;[Cu(NH3)4]2+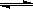 Cu2++4NH3。请写出在CuSO4溶液中逐滴加入氨水至过量的反应现象: 。
Cu2++4NH3。请写出在CuSO4溶液中逐滴加入氨水至过量的反应现象: 。
(3)①方案1的实验步骤为:加热蒸发→冷却结晶→过滤洗涤→干燥。该方案存在明显缺陷,因为得到的产物晶体往往含有Cu2(OH)2SO4杂质,产生该杂质的原因是 。
②方案2是较为理想的结晶方案,先向溶液C加入适量 (填物质名称),再过滤、洗涤、干燥即可得到较纯净的晶体。下列选项中,最适合作为滤出晶体洗涤液的是 。
A.乙醇 B. 蒸馏水 C.乙醇和水的混合液 D.饱和硫酸钠溶液
洗涤沉淀的操作方法是 。
(4)氨含量的测定:准确称取a g络氨铜样品,加入过量NaOH溶液微热,使NH3充分释放,并被准确量取的30.00mL 0.5000mol.L-1HCl溶液充分吸收。吸收液用0.1200mol·L-1的NaOH溶液滴定,消耗的NaOH溶液的体积为V L,则络氨铜样品中氨的质量分数为 (用含a、V的字母表达)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期10月月考化学试卷(解析版) 题型:选择题
将5 mol/L盐酸10 mL稀释到200 mL,再取出5 mL,这5 mL溶液的物质的量浓度是
A.0.05 mol/L B.0.25 mol/L C.0.1 mol/L D.0.5 mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省台州市高一上学期第一次月考化学试卷(解析版) 题型:实验题
右图所示装置有多种用途,请回答下列问题:
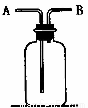
(1)洗气:除去CO中的水蒸气,装置内应盛放 ;
(2)检验:证明CO中混有CO2,装置内应盛放 ;
(3)集气:若用排空气法收集比空气轻的气体时,气体应从装置的 端通入(填“A” 或“B”,下同);若收集比空气重的气体,则气体从 端通入。若用排水法收集O2时,瓶内应先装满水,气体从 端通入。
(4)贮气:若要用水将装置中的氧气排出进行实验时,水应从 端通入。
(5)量气:若要测定实验室制得的少量O2的体积,则应在瓶内先装满水,再将O2从 端通入。
查看答案和解析>>
科目:高中化学 来源:2016届河南省顶级名校高三上学期期中测试化学试卷(解析版) 题型:填空题
聚合氯化铝是新型、高效絮凝剂和净水剂,其单体是液态碱式氯化铝[Al2(OH)nCl6-n]。工业上常采用铝盐溶液部分水解制备碱式氯化铝,其工艺流程如下:
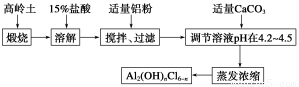
已知:高岭土:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)及少量杂质和水。Al3+以氢氧化物形式完全沉淀时,溶液的pH为5.2。根据流程图回答下列问题:
(1)写出溶解过程中反应的离子方程式________________________;
(2)加适量铝粉的主要目的是_________________________________。
(3)溶液的pH需控制在4.2~4.5的原因是__________________,__________________。
(4)“蒸发浓缩”需保持温度在90~100 ℃,控制该温度的操作名称是____________,写出该过程反应的化学方程式______________________。
查看答案和解析>>
科目:高中化学 来源:2016届四川省绵阳市高三上学期第一次诊断性测试理综化学试卷(解析版) 题型:选择题
七种短周期元素在元素周期表中的相对位置如表所示。其中B的最高价氧化物的水化物能与B的气态氢化物反应生成离子化合物,下列说法正确的是

A.氧化物对应的水化物的酸性:G一定强于F
B.简单离子的半径:F>G>C>D
C.1 mol EC2中含2 mol E-C键
D.A、G分别与氢元素形成的化合物中,化学键均为极性共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com