
| A. | 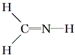 | B. | 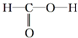 | C. | 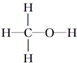 | D. | 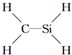 |
分析 根据非金属元素之间易形成共价键,原子间形成共价键而达到稳定结构,氮原子能形成3个共价键,碳原子、硅原子能形成4个共价键,氧原子、硫原子、硒原子能形成2个共价键,氢原子能形成1个共价键,氧原子能形成2个共价键进行分析.
解答 解:A. 中每个氢原子能形成1个共价键,氮原子能形成3个共价键,碳原子能形成4个共价键,所以每个原子都达到稳定结构,故A正确;
中每个氢原子能形成1个共价键,氮原子能形成3个共价键,碳原子能形成4个共价键,所以每个原子都达到稳定结构,故A正确;
B.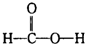 中碳原子能形成4个共价键,氧原子能形成2个共价键,从而使各个原子能达到稳定结构,故B正确;
中碳原子能形成4个共价键,氧原子能形成2个共价键,从而使各个原子能达到稳定结构,故B正确;
C.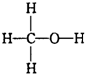 中每个碳原子能形成4个共价键,氢原子能形成1个共价键,氧原子能形成2个共价键,从而使各个原子能达到稳定结构,故C正确;
中每个碳原子能形成4个共价键,氢原子能形成1个共价键,氧原子能形成2个共价键,从而使各个原子能达到稳定结构,故C正确;
D.碳原子、硅原子能形成4个共价键,而 中碳原子、硅原子成键情况不合理,故D错误;
中碳原子、硅原子成键情况不合理,故D错误;
故选:D.
点评 本题考查了化学键的判断,明确每个原子价层电子数和成键数目是解本题关键,难度不大.


科目:高中化学 来源: 题型:解答题

| 实验编号 | 待测液体积 (mL) | 消耗盐酸体积(mL) | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.00 | 25.02 |
| 2 | 20.00 | 0.20 | 28.80 |
| 3 | 20.00 | 1.30 | 26.28 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化氢气体不能导电,所以氯化氢不是电解质 | |
| B. | SO2溶于水形成的溶液能导电,所以SO2是电解质 | |
| C. | 碳棒能导电但属于非电解质 | |
| D. | 电解质不一定能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Al3+)=0.1mol/L的溶液中:Na+、K+、HS-、SO42- | |
| B. | 使酚酞呈红色的溶液中:K+、Ba2+、I-、NO3- | |
| C. | 由水电离出的c(H+)=10-13mol/L的溶液中:Na+、HCO3-、Cl-、Br- | |
| D. | 加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①② | C. | ①③ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.T1℃时,在1L密闭容器中充入0.6molSO3,如图表示SO3物质的量随时间的变化曲线.
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.T1℃时,在1L密闭容器中充入0.6molSO3,如图表示SO3物质的量随时间的变化曲线.| T/℃ | T2 | T3 |
| K | 20.5 | 4.68 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将SO2通入Ba(NO3)2溶液中能生成BaSO4沉淀 | |
| B. | 在Si02+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2C0的反应中,Si02是氧化剂 | |
| C. | 生铁在潮湿的空气中主要发生析氢腐蚀 | |
| D. | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色气体,说明该钾盐是K2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜片上出现铜绿[Cu2(OH)2CO3] | B. | 铁制菜刀生锈 | ||
| C. | 铝锅表面生成致密的氧化膜 | D. | 用醋清理水垢 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com