
科学家一直致力于研究常温、常压下“人工固氮”的新方法。曾有实验报道:在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。进一步研究NH3生成量与温度的关系,部分实验数据见下表(光照、N2、压强1.0×105 Pa、反应时间3 h):
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量 /10-6 mol | 4.8 | 5.9 | 6.0 | 2.0 |
相应的热化学方程式如下:
N2(g)+3H2O(l)===2NH3(g)+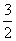 O2(g)
O2(g)
ΔH=+765.2 kJ·mol-1
回答下列问题:
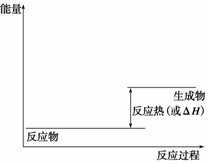
(1)请画出上述反应在有催化剂与无催化剂两种情况下反应过程中体系能量变化的示意图,并进行必要标注。
(2)与目前广泛使用的工业合成氨方法相比,该方法固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议:
________________________________________________________________________。
(3)工业合成氨的反应为N2(g)+3H2(g)
 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为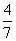 。计算:
。计算:
①该条件下N2的平衡转化率;
②该条件下反应2NH3(g)
 N2(g)+3H2(g)的平衡常数。
N2(g)+3H2(g)的平衡常数。
答案 (1)

(2)升温、增大N2浓度、不断移出生成物
(3)①66.7% ②5.0×10-3
解析 (1)催化剂能降低反应的活化能,改变反应的历程,使一个高能变过程变为几个能量相对低的过程,使反应易发生。要点是有催化剂时能量低而过程阶段多了。图见答案。
(2)加快反应速率且增大NH3生成量的方法是升温、增大N2浓度、不断移出生成物。
(3)①设反应过程中消耗了x mol N2(g)。
N2(g) + 3H2(g)
 2NH3(g)
2NH3(g)
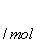 0.60 1.60 0
0.60 1.60 0
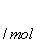 0.60-x 1.60-3x 2x
0.60-x 1.60-3x 2x
平衡时反应体系中总物质的量=[(0.60-x)+(1.60-3x)+2x] mol=(2.20-2x) mol
NH3(g)的物质的量分数= =
=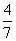
x=0.40
N2的平衡转化率=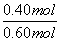 ×100%=66.7%
×100%=66.7%
① 设反应2NH3(g)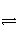
 N2(g)+3H2(g)的平衡常数为K。平衡时,c(NH3)=2×0.40 mol÷2.0
N2(g)+3H2(g)的平衡常数为K。平衡时,c(NH3)=2×0.40 mol÷2.0
L=0.40 mol·L-1
c(N2)=(0.60-0.40) mol÷2.0 L=0.10 mol·L-1
c(H2)=(1.60-3×0.40) mol÷2.0 L=0.20 mol·L-1
K=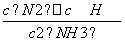 =0.10×(0.20)3÷(0.40)2
=0.10×(0.20)3÷(0.40)2
=5.0×10-3


科目:高中化学 来源: 题型:
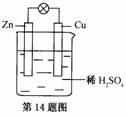 如图为铜锌原电池示意图,下列说法不正确的是
如图为铜锌原电池示意图,下列说法不正确的是
A.该原电池中,铜为正极
B.该原电池中,电子由铜片经过导线流入锌片
C.该原电池工作一段时间后,溶液的酸性减弱
D.该原电池工作一段时间后,锌片质量减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列能用勒夏特列原理解释的是( )
A.高温及加入催化剂都能使合成氨的反应速率加快
B.红棕色的NO2加压后颜色先变深后变浅
C.SO2催化氧化成SO3的反应,往往需要使用催化剂
D.H2、I2、HI平衡时的混合气体加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)估计下列各变化过程是熵增还是熵减。
①NH4NO3爆炸:2NH4NO3(s)===2N2(g)+4H2O(g)+O2(g)
②水煤气转化:CO(g)+H2O(g)===CO2(g)+H2(g)
③臭氧的生成:3O2(g)===2O3(g)
(2)可逆反应A(g)+B(g)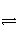
 2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。
2C(g)在不同温度下经过一定时间,混合物中C的体积分数与温度的关系如图所示。
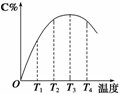
①由T1向T2变化时,正反应速率______逆反应速率(填“>”、“<”或“=”)。
②由T3向T4变化时,正反应速率______逆反应速率(填“>”、“<”或“=”)。
③反应在________温度下达到平衡。
④此反应的正反应为______热反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气是一种重要的工业原料。工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是 ( )
A.若管道漏气遇氨就会产生白烟 B.该反应利用了Cl2的强氧化性
C.该反应属于复分解反应 D.生成1molN2有6mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
运用元素周期律分析下面的推断,其中不正确的是 ( )
A.锂(Li)与水反应比钠与水反应剧烈
B.砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸
C.在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂
D.HBrO4的酸性比HIO4的酸性强
查看答案和解析>>
科目:高中化学 来源: 题型:
农药在农业生产中起到了重要的作用,有机物D是生产农药的中间体,下图是由A合成有机物D的生产流程。

已知:
(1)A为苯的同系物,其含氢的质量分数与甘油的相等,则A的结构简式是_________。
(2)有机物C通过连续氧化可以得到一种羧酸E,C与E发生化学反应的方程式是 ;
有机物C还具有的性质有_________
a、能与氢氧化钠反应 b、能与浓氢溴酸反应c、能发生消去反应d、能发生加成反应
(3)请写出符合下列要求E的同分异构体的结构简式:
①苯环上只有一个取代基的结构简式为 ;
②苯环上有两个取代基,且该分子核磁共振氢谱图上有四个吸收峰的结构简式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com