
【题目】下列过程的能量变化符合下图所示的是
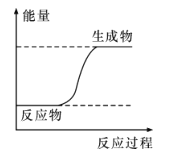
A. 酸碱中和反应
B. CH4在O2中燃烧
C. NH4Cl晶体与Ba(OH)28H2O晶体混合搅拌
D. CaO溶于水生成Ca(OH)2
科目:高中化学 来源: 题型:
【题目】葡萄糖酸亚铁(C6H11O7) 2Fe是常用的补铁剂,易溶于水。用下图装置制备 FeCO3,提取出的 FeCO3与葡萄糖酸反应可得葡萄糖酸亚铁。回答下列问题:

Ⅰ.(1)如何检验 A 装置的气密性?____。
(2)B中加入药品Na2CO3,要使A中制得的FeSO4溶液进入B中发生反应,实验开始时,应打开分液漏斗的活塞、______,关闭_____,一段时间后,关闭_______,打开_____(填旋塞的编号)。
(3)将制得的碳酸亚铁悬浊液过滤、洗涤。如何证明沉淀已经洗涤干净_________。
(4)将葡萄糖酸与碳酸亚铁混合,反应的化学方程式为(有机物用分子式表示)_____。
(5)从环境保护的角度分析,该装置存在不足之处,请写出改正措施__________。
Ⅱ.某补铁剂的主要成分是硫酸亚铁,用氧化还原滴定法可测定该补铁剂中铁元素的含量,实验的主要步骤如下:
①取10片补铁剂样品,溶解除去不溶物(不损耗铁元素),并配成100mL待测溶液。
②量取20.00mL待测液于锥形瓶中。
③用cmol·L1的酸性KMnO4溶液滴定至终点,记录消耗KMnO4溶液的体积,重复两次实验,平均消耗KMnO4溶液体积为VmL。
(6)上述实验中应该用稀硫酸酸化KMnO4溶液,如果用硝酸对KMnO4溶液进行酸化,对测定结果的影响是_____(填“偏大”“偏小”或“无影响”)。滴定终点的实验现象为_____。
(7)每片补铁剂含铁元素的质量为________________g(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学课外小组用图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
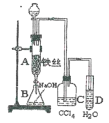
(1)写出A中反应的化学方程式_______________。
(2)观察到A中的现象是_____________________。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是________,写出有关的化学方程式______________________________。
(4)C中盛放CCl4的作用是________________。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入_______,现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,正确的是
A. 用惰性电极电解MgCl2溶液:2Cl—+H2O ![]() 2OH—+Cl2↑+H2↑
2OH—+Cl2↑+H2↑
B. SO2通入碘水中,反应的离子方程式为SO2+I2+2H2O=SO42-+2I-+4H+
C. 氯气通入冷水中:Cl2 +H2O ![]() Cl- +ClO- +2H+
Cl- +ClO- +2H+
D. Na2S溶液中![]() 的水解:S2—+2H2O==H2S+2OH—
的水解:S2—+2H2O==H2S+2OH—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生用如图所示装置进行实验,以探究苯与溴发生反应的原理并分离提纯反应的产物![]() 请回答下列问题:
请回答下列问题:

(1)冷凝管所起的作用为冷凝回流蒸气,冷凝水从 ____![]() 填“a”或“b”
填“a”或“b”![]() 口进入。
口进入。
(2)实验开始时,关闭![]() 、开启
、开启![]() 和分液漏斗活塞,滴加苯和液溴的混合液,反应开始,III中小试管内苯的作用是__________ 。
和分液漏斗活塞,滴加苯和液溴的混合液,反应开始,III中小试管内苯的作用是__________ 。
(3)能说明苯与液溴发生了取代反应的现象是_____________ ;若把III中洗气瓶内的硝酸银溶液换为 ______![]() 填试剂名称
填试剂名称![]() ,当出现______________ 现象也能说明发生取代反应。
,当出现______________ 现象也能说明发生取代反应。
(4)四个实验装置中能起到防倒吸的装置有_________________ 。
(5)将三颈烧瓶内反应后的液体依次进行下列实验操作就可得到较纯净的溴苯。
![]() 用蒸馏水洗涤,振荡,分液;
用蒸馏水洗涤,振荡,分液;![]() 用
用![]() 的NaOH溶液洗涤,振荡,分液;
的NaOH溶液洗涤,振荡,分液;![]() 用蒸馏水洗涤,振荡,分液;
用蒸馏水洗涤,振荡,分液;![]() 加入无水氯化钙干燥;
加入无水氯化钙干燥;![]() ______
______![]() 填操作名称
填操作名称![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家研发出一种新型水溶液锂电池,采用复合膜包裹的金属锂作负极,锰酸锂(LiMn2O4)作正极,以0.5 mol/Li2SO4 水溶液作电解质溶液。电池充、放电时,LiMn2O4与Li2Mn2O4可以相互转化。下列有关该电池的说法正确的是
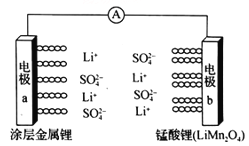
A. 该电池放电时,溶液中的SO42-向电极b移动
B. 该电池负极的电极反应式为:2Li+2H2O==2LiOH+H2↑
C. 电池充电时,外加直流电源的正极与电极a相连
D. 电池充电时,阳极的电极反应式为:Li2Mn2O4-e-==LiMn2O4 +Li+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语中,正确的是( )
A.CCl4的电子式为![]()
B.CaCl2的电子式为![]()
C.HClO的结构式为H—Cl—O
D.用电子式表示HCl的形成过程为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一容积不变的密闭容器中发生可逆反应2X(g) ![]() Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
A. 混合气体的密度不再变化 B. 反应容器中Y的质量分数不变
C. X的分解速率与Y的消耗速率相等 D. 单位时间内生成1 mol Y的同时生成2 mol X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂利用工业废水M(含有MgSO4、NaCl、MnSO4)为原料制备氮镁磷复合肥MAP,其生成流程如图所示:
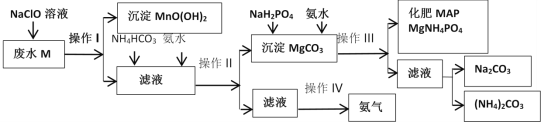
回答下列问题:
(1)实验室中,操作I、II、III为过滤,过滤所需的玻璃仪器有___;若发现滤液浑浊,可能的原因是___;洗涤沉淀的操作是___。
(2)废水M中加入NaClO溶液发生反应的离子方程式为___。
(3)化工生产中,若针对操作IV,欲获得氨气,用于化工生产循环利用,该操作为___。
(4)化肥MAP生产过程中,加入NaH2PO4和氨水,此时氨水的作用是___。
(5)写出操作III中形成化肥MAP的化学反应方程式为___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com