
| A. | CuSO4只是还原剂 | |
| B. | Cu3P既是氧化产物又是还原产物 | |
| C. | P既是氧化剂又是还原剂 | |
| D. | 若有11 mol P参加反应,转移电子的物质的量为60 mol |
分析 11P+15CuSO4+24H2O═5Cu3P+6H3PO4+15H2SO4中,P元素的化合价由0降低为-3价,P元素的化合价由0升高为+5价,Cu元素的化合价由+2价降低为+1价,以此来解答.
解答 解:A.Cu元素化合价降低,CuSO4为氧化剂,故A错误;
B.P元素的化合价由0升高为+5价,P是还原剂,H3PO4是氧化产物,Cu3P是还原产物,故B错误;
C.反应中P的化合价分别由0价变为-3价、+5价,则既是氧化剂又是还原剂,故C正确;
D.由原子守恒可知,11molP参加反应,被氧化的P为6mol,则转移的电子为6mol×5=30mol,故D错误;
故选C.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,注意从元素的化合价角度分析,题目难度不大.


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:选择题
| A. | 纯的金属在有水的溶液中比不纯的金属(或合金)在其中更容易发生腐蚀 | |
| B. | 金属根据接触的介质的不同,发生腐蚀的化学原理分为:化学腐蚀和电化学腐蚀 | |
| C. | 铝不需要特别的处理就具有抗腐蚀能力 | |
| D. | 在轮船在装上一块锌可以起到保护船身的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
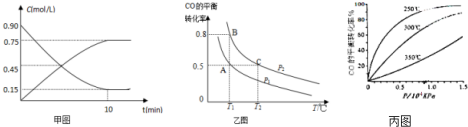
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
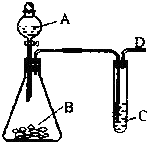 某同学用如图所示的装置来探究SO2的性质及有关实验.
某同学用如图所示的装置来探究SO2的性质及有关实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧燃料电池工作时,1mol H2在正极上失去2mol电子 | |
| B. | 0.1mol/LNa2CO3溶液加热后,溶液的CO32-的数目小于6.02×1022个 | |
| C. | 常温常压下,22.4LCl2中含有的分子数为6.02×1023个 | |
| D. | 室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ②③⑤ | C. | ①②⑤ | D. | ①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com