
����Ŀ���й�������Լ���ƴ������ʱ����������¯��ʯ�㻯�Bʯ(���Bʯ��)�ļ��գ���¯��ʯ(ZnCO3)����ͭ��(��Ҫ�ɷ�Cu2O)��ľ̿�ۻ�ϼ�����800�����ҿ��Ƶ���ƽ����Ƶ��Bʯ�𡣻ش��������⣺
(1)пԪ�ػ�̬ԭ�ӵļ۵����Ų�ʽΪ________________��ͭԪ�ػ�̬ԭ���е�δ�ɶԵ�����Ϊ_________________��
(2)����п���ڹ�����ˮ�γ�[Zn(NH3)4]SO4��Һ��
��[Zn(NH3)4]SO4�У������ӵ����幹����__________________��[Zn(NH3)4]2+�к��еĻ�ѧ����__________________��
��NH3�����У�����ԭ�ӵĹ���ӻ�����Ϊ________________��NH3��H2O�е��ܽ��____________(���С��)��ԭ����_____________________��
(3)ͭ�ĵ�һ������ΪI1Cu=745.5kJ��mol-1���ڶ�������ΪI2Cu=1957.9kJ��mol-1��п�ĵ�һ������ΪI1Zn=906.4kJ��mol-1���ڶ�������ΪI2Zn=1733.3kJ��mol-1��I2Cu>I2Zn��ԭ����___________________��
(4)Cu2O����ľ����ṹ��ͼ��ʾ��O2-����λ��Ϊ_______________����Cu2O���ܶ�Ϊdg��cm-3��������a=____________nm��

���𰸡� 3d104s2 1 �������� ��λ���ͼ��Թ��ۼ� sp3 �� NH3���Ӻ�H2O���Ӿ�Ϊ���Է��ӣ���NH3���Ӻ�H2O����֮�����γ���� ͭʧȥ����ȫ������3d10���ӣ���пʧȥ����4s1���� 4 ![]() ��107
��107
����������������1��Znԭ�Ӻ�����30�����ӣ����ݹ���ԭ��д����̬Zn�ĺ�������Ų�ʽ������д���۵����Ų�ʽ��Cu��̬ԭ����δ�ɶԵ�����Ϊ1����
��2�������ݼ۲���ӶԻ�������ȷ��SO42-�����幹����Zn2+��NH3���Ӽ�Ϊ��λ����NH3�����ں����Թ��ۼ���
��NH3������NΪsp3�ӻ���NH3���Ӻ�H2O���Ӷ��Ǽ��Է��ӣ�NH3���Ӻ�H2O���Ӽ��γ������NH3��H2O�е��ܽ�ȴ�
��3���ӵ����Ų�ʽ���ȶ����Ϸ�����
��4��������̯����ȷ�����������ĸ�������1mol������������ܶȼ���1mol������������1mol���������;��������ĸ�����NA���㾧����������������㾧��������
�������1��Znԭ�Ӻ�����30�����ӣ����ݹ���ԭ������̬Znԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s23p63d104s2����̬Znԭ�ӵļ۵����Ų�ʽΪ3d104s2��Cuԭ�Ӻ�����29�����ӣ���̬Cuԭ�Ӻ�������Ų�ʽΪ1s22s22p63s23p63d104s1��4s����1��δ�ɶԵ��ӣ�����̬Cuԭ����1��δ�ɶԵ��ӡ�
��2����SO42-������ԭ��S�ϵŵ��Ӷ���=![]() ��6+2-4
��6+2-4![]() 2��=0���ɼ����Ӷ���Ϊ4���۲���Ӷ���Ϊ0+4=4��VSEPRģ��Ϊ���������ͣ�S��û�йµ��Ӷԣ�SO42-�����幹��Ϊ����������[Zn��NH3��4]2+��Zn2+��NH3���Ӽ�Ϊ��λ����NH3�����ں����Թ��ۼ���
2��=0���ɼ����Ӷ���Ϊ4���۲���Ӷ���Ϊ0+4=4��VSEPRģ��Ϊ���������ͣ�S��û�йµ��Ӷԣ�SO42-�����幹��Ϊ����������[Zn��NH3��4]2+��Zn2+��NH3���Ӽ�Ϊ��λ����NH3�����ں����Թ��ۼ���
��NH3����������ԭ��N�ļ۲���Ӷ���=![]() ��5-3
��5-3![]() 1��+3=4��Nԭ�Ӳ�ȡsp3�ӻ���NH3���Ӻ�H2O���Ӷ��Ǽ��Է��ӣ�������������������NH3���Ӻ�H2O���Ӽ��γ����������NH3��H2O�е��ܽ�ȴ�
1��+3=4��Nԭ�Ӳ�ȡsp3�ӻ���NH3���Ӻ�H2O���Ӷ��Ǽ��Է��ӣ�������������������NH3���Ӻ�H2O���Ӽ��γ����������NH3��H2O�е��ܽ�ȴ�
��3����̬Cuԭ�ӵļ۵����Ų�ʽΪ3d104s1����̬Znԭ�ӵļ۵����Ų�ʽΪ3d104s2��Cu�ĵڶ�������ʧȥ����ȫ������3d10���ӣ�Zn�ĵڶ�������ʧȥ����4s1���ӣ�����I2Cu![]() I2Zn��
I2Zn��
��4���ɾ������Կ���O2-����λ��Ϊ4���á���̯������1�������к�O2-��8![]() +1=2����Cu+��4����1molCu2O������Ϊ144g��1mol��������Ϊ144g
+1=2����Cu+��4����1molCu2O������Ϊ144g��1mol��������Ϊ144g![]() dg/cm3=
dg/cm3=![]() cm3��1�����������Ϊ
cm3��1�����������Ϊ![]() cm3
cm3![]() NA
NA![]() 2=
2=![]() cm3����������a=
cm3����������a=![]() cm=
cm=![]() 107nm��
107nm��


 ����ͼ���������������ϵ�д�
����ͼ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�ѧ����������ȷ����( )
A.���ӻ�������ܺ����ۼ������ۻ������в������Ӽ�
B.���ۻ�������ܺ����Ӽ������ӻ�������ֻ�����Ӽ�
C.���ɵ��ʷ��ӵ���һ�����й��ۼ�
D.���Ȼ����У�ֻ���������Ӻ������ӵľ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������½�NaOH��Һ�μӵ�������(H2SeO3)��Һ�У������Һ��pH������Ũ�ȱ仯�Ĺ�ϵ��ͼ��ʾ������������ȷ����
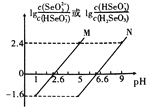
A. Ka1(H2SeO3)��������Ϊ10-7
B. ����M��ʾpH��lg![]() �ı仯��ϵ
�ı仯��ϵ
C. NaHSeO3��Һ��c(OH-)>c(H+)
D. �����Һ�У�lg![]() - lg
- lg![]() =lgKa1(H2SeO3)-lgKa2(H2SeO3)=4
=lgKa1(H2SeO3)-lgKa2(H2SeO3)=4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��ͨ������SiO2 ��̼��Ӧ����ȡ�裬д����Ӧ�Ļ�ѧ����ʽ___________________��
��ҵ�ϻ���������þ��ȡ�裬��ӦΪ2Mg+SiO2 = 2MgO+Si��ͬʱ�ᷢ������Ӧ��2Mg + Si = Mg2Si����ͼ�ǽ���Mg��SiO2��Ӧ��ʵ��װ�ã��Իش��������⣺

��1������O2��H2O��g���Ĵ��ڶԸ�ʵ���нϴ�Ӱ�죬ʵ����Ӧͨ������X��Ϊ���������Թ��еĹ���ҩƷ��ѡ��________(�����)��
a��ʯ��ʯ������b��п��������c������
��2��ʵ�鿪ʼʱ��������ͨһ��ʱ��X���壬�ټ��ȷ�Ӧ��������� ___________________________������Ӧ���������߾ƾ��ƣ���Ӧ�ܼ������У���ԭ����______________________��
��3����Ӧ��������ȴ������ʱ������Ӧ��Ļ�����м���ϡ���ᣬ�ɹ۲쵽�����Ļ��ǣ������������ԭ���Ǹ�����Mg2Si������Ѹ�ٷ�Ӧ����SiH4�����飩���壬Ȼ��SiH4��ȼ���û�ѧ����ʽ��ʾ��������Ӧ��________________________��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������(��)���Ҷ�ȩ������ȩ���ǻ���ԭ�ϣ�ijС����Ƶĺϳ�·�����£�
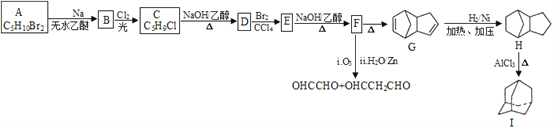
��֪��
��2R-Br+2Na![]() R-R+2NaBr
R-R+2NaBr
��B�ĺ˴Ź�������ֻ��1�����շ�
��![]()
��![]()
�ش��������⣺
(1)A�Ļ�ѧ����Ϊ_____________�� D�Ľṹ��ʽΪ__________________��I�ķ���ʽΪ__________________��
(2)B��C�Ļ�ѧ����ʽ_________________��E��F�Ļ�ѧ����ʽΪ_______________���÷�Ӧ����Ϊ________________��
(3)G�ķ�����ͬ���칹���У������ϵ�ȡ������ĿС��3����ʹ������Ȼ�̼��Һ��ɫ�Ĺ���_______��(���������칹)�����к˴Ź���������5��壬�ҷ������Ϊ6��2��2��1��1����_________________(д�ṹ��ʽ)��
(4)д���û����ϩ����ϩΪԭ���Ʊ�������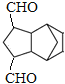 �ĺϳ�·��____________(�����Լ���ѡ)��
�ĺϳ�·��____________(�����Լ���ѡ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�б�����뻹ԭ�����ܽ��е��ǣ�������
A.MnO4����Mn2+
B.Cl2��Cl��
C.H2��H2O
D.Zn��Zn2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǹ�ˮ����[Cr(CH3COO)2]2��2H2O��һ���������ռ���Ϊ����ɫ���塣��ʪ�������ױ������������Ҵ�,������ˮ������(�ӷ����л��ܼ���������ˮ)�����Ʊ�װ�ü���������:

�ټ��װ��������,��������ƿ�����μ������п�ۣ�200mL0.200mol/LCrC13��Һ��
�ڹر�k2��k1,������Һ©�������������ƺõ��١�
�۴�������ƿ�ȵ���Һ������ɫ(Cr3+)��Ϊ����ɫ(Cr2+)ʱ������Һת�Ƶ�װ�����С������ִ�������ɫƷ��ʱ���رշ�Һ©����������
�ܽ�װ�����л������ٹ��ˡ�ϴ�Ӻ�������õ�5.64g[Cr(CH3COO)2]2��2H2O
��1��װ�ü�����ͨ��a��������________����μ����װ�õ��������Ƿ�����?__________��
��2��������ƿ�е�Zn��������������H2�⣬��������һ����Ӧ�����ӷ���ʽΪ__________��
��3�����������Һ�Զ�ת����װ�����е�ʵ�����Ϊ________________��
��4��װ�ñ���������________________��
��5��������н���ϴ�ӵIJ�������Ϊ________________________________��
��6��ϴ�Ӳ�Ʒʱ�����֤����Ʒ�Ѿ�ϴ�Ӹɾ�?______________________��
��7����ʵ����[Cr(CH3COO)2]2��2H2O (��Է�������Ϊ376)�IJ�����___��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com