
| A. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | B. | S2-的结构示意图: | ||
| C. | CaO2的电子式: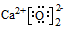 | D. | 葡萄糖的结构简式:C6H12O6 |
分析 A、质量数写在原子符号的左上角,且质量数=质子数+中子数;
B、硫离子是硫原子得2个电子形成的;
C、根据过氧化钙构成离子是钠离子和过氧根离子分析;
D、葡萄糖为多羟基醛,含有5个羟基一个醛基.
解答 解:A、质量数写在原子符号的左上角,且质量数=质子数+中子数,故中子数为20的氯原子的质量数为37,故符号为3717Cl,故A错误;
B、硫离子是硫原子得2个电子形成的,故硫离子的核外有18个电子,故结构示意图为 ,故B正确;
,故B正确;
C、过氧化钙构成离子是钠离子和过氧根离子,过氧化钙为离子化合物,钙离子直接写成离子形式,过氧根离子需要标出最外层电子,过氧化钙的电子式为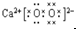 ,故C错误;
,故C错误;
D、葡萄糖为多羟基醛,含有5个羟基一个醛基,故结构简式为:CH2OHCHOHCHOHCHOHCHOHCHO,故D错误.
故选B.
点评 本题考查常见的化学用语和有机物的结构简式,明确有机物的结构是解答本题的关键,题目难度不大.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $→_{②}^{NaOH,乙醇,△}$
$→_{②}^{NaOH,乙醇,△}$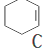 $→_{③}^{溴CCl_{4}溶液}$D$\stackrel{④}{→}$
$→_{③}^{溴CCl_{4}溶液}$D$\stackrel{④}{→}$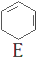
 ,名称是环己烷;
,名称是环己烷; ;B水解的化学方程式为
;B水解的化学方程式为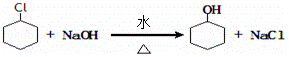 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100g质量分数为46%的乙醇水溶液中氧原子数为4NA | |
| B. | 1molCl2通入水中,HClO、Cl-、ClO-粒子数之和小于2 NA | |
| C. | 标准状况下,2.24LD2中所含中子的数目是0.2NA | |
| D. | 25℃时,KSP(BaSO4)=l×10-10,则BaSO4饱和溶液中Ba2+数目为l×10-5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 为保护环境,应减少二氧化硫、氮氧化物和二氧化碳等物质的排放量.
为保护环境,应减少二氧化硫、氮氧化物和二氧化碳等物质的排放量.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向2mL10%的NaOH溶液中滴加2%CuSO4溶液4~6滴制得新制氢氧化铜悬浊液 | |
| B. | 将Al2(SO4)3溶液蒸干、灼烧至恒重,最终剩余固体是Al2O3 | |
| C. | 将水蒸气通过灼热的铁粉,铁粉变红棕色,说明铁与水在高温下能发生反应 | |
| D. | 取a克Na2CO3和NaHCO3混合物与少量稀盐酸充分反应,加热、蒸干、灼烧至熔化,冷却得b克固体,可测得Na2CO3质量分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,向100mL 0.01mol•L-1 MOH溶液中逐滴加入0.02mo1•L-1 HA溶液,图中所示曲线表示混合溶液的pOH变化情况(溶液体积变化忽略不计),溶液中pOH=-lgc(OH-).下列说法中,不正确的是( )
常温下,向100mL 0.01mol•L-1 MOH溶液中逐滴加入0.02mo1•L-1 HA溶液,图中所示曲线表示混合溶液的pOH变化情况(溶液体积变化忽略不计),溶液中pOH=-lgc(OH-).下列说法中,不正确的是( )| A. | MOH为一元强碱 | |
| B. | N点水的电离程度大于K点水的电离程度 | |
| C. | 该温度下HA的电离平衡常数为5×10-6mo1•L-1 | |
| D. | 若K点对应溶液的pOH=10,则有c(HA)+c(H+)-c(OH-)=0.01mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广使用清洁能源 | B. | 大力发展燃煤发电 | ||
| C. | 循环高效利用费源 | D. | 倡导环保低碳生活 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com