
【题目】X、Y、Z、Q、R为原子序数依次增大的短周期元素。25℃时,其最高价氧化物的水化物溶液(浓度均为0.001mol·L-1)的pH和原子半径的关系如图所示。下列说法中正确的是( )
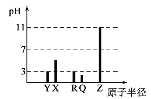
A.Y和Z的简单离子半径:Y<Z
B.R、Q的气态氢化物的稳定性:R>Q
C.R的最高价氧化物对应水化物的化学式为HRO3
D.上述五种元素中有两种元素是金属元素
【答案】B
【解析】
X、Y、Z、Q、R为原子序数依次增大的短周期元素,由25℃时,其最高价氧化物的水化物溶液(浓度均为0.001mol·L-1)的pH和原子半径的关系示意图可知,Z的原子半径最大,且最高价氧化物的水化物为强碱,则Z为Na元素;Q的最高价氧化物的水化物为二元强酸,则Q为S元素;Y、R的最高价氧化物的水化物为一元强酸,则Y为N元素、R为Cl元素;X的原子序数小于Y、原子半径大于Y,且最高价氧化物的水化物为弱酸,则X为C或B元素。
A. 具有相同的电子层结构的离子,随核电荷数增大,离子半径依次减小,氮离子和钠离子具有相同的电子层结构,则氮离子半径大于钠离子,故A错误;
B.元素的非金属性越强,气态氢化物的稳定性越强,则氯化氢比硫化氢稳定,故B正确;
C.氯元素的最高价氧化物对应水化物的化学式为HClO4,故C错误;
D. X、Y、Z、Q、R五种元素中只有钠元素是金属元素,故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】N2H4是一种高效清洁的火箭燃料。已知在25℃、101kPa下,8gN2H4(g)完全燃烧生成氮气和液态水时,放出133.5 kJ热量。则下列热化学方程中正确的是( )
A. N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534kJ·mol-1
B. N2H4(g)+O2(g)=N2(g)+2H2O(l) △H=-133.5kJ·mol-1
C. N2H4(g)+O2(g)=N2(g)+2H2O(l) △H=+534kJ·mol-1
D. N2H4(g)+O2(g)=N2(g)+2H2O(l) △H=-534kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是
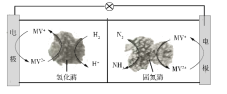
A. 相比现有工业合成氨,该方法条件温和,同时还可提供电能
B. 阴极区,在氢化酶作用下发生反应H2+2MV2+![]() 2H++2MV+
2H++2MV+
C. 正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D. 电池工作时质子通过交换膜由负极区向正极区移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气环境中![]() 的减量化排放受到国内外广泛关注。利用碳还原NO的反应为:
的减量化排放受到国内外广泛关注。利用碳还原NO的反应为:![]() 。回答下列问题:
。回答下列问题:
(1)该反应在常温下可以自发进行,则反应的![]() ________0(填“
________0(填“![]() ”“
”“![]() ”或“
”或“![]() ”),有利于提高NO平衡转化率的条件是________(任写一条)。
”),有利于提高NO平衡转化率的条件是________(任写一条)。
(2)以上反应可分为如下四步反应历程,写出其中第三步的反应:
第一步:![]()
第二步:![]()
第三步:________
第四步:![]()
(3)对比研究活性炭负载钙、镧氧化物的反应活性。在三个反应器中分别加入C、![]() 、
、![]() ,通入
,通入![]() 使其浓度达到
使其浓度达到![]() 。不同温度下,测得第2小时NO去除率如图所示:
。不同温度下,测得第2小时NO去除率如图所示:
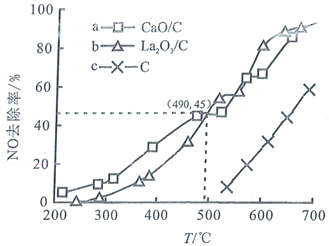
①据图分析,490℃以下,三种情况下反应的活化能最小的是________(用a、b、c表示);![]() 、
、![]() 去除NO效果比C更好,其依据是________(写一条)。
去除NO效果比C更好,其依据是________(写一条)。
②上述实验中,490℃时,若测得![]() 对NO的去除率为60%,则可能采取的措施是________。
对NO的去除率为60%,则可能采取的措施是________。
A.及时分离出![]() B.压缩体积
B.压缩体积
C.恒容下,向体系中通入氮气 D.寻找更好的催化剂
③490℃时的反应速率![]() ________
________![]() ,该温度下此反应的平衡常数为121,则反应达平衡时NO的去除率为________(保留二位有效数字)。
,该温度下此反应的平衡常数为121,则反应达平衡时NO的去除率为________(保留二位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国中草药文化源远流长,通过临床试验,从某中草药中提取的有机物具有较好的治疗癌症的作用,该有机物的结构如图所示。下列说法中错误的是( )

A.分子式为C13H12O6
B.该有机物能发生取代反应、加成反应、氧化反应
C.1mol该有机物与NaOH反应最多消耗2molNaOH
D.1mol该有机物与溴水反应最多消耗3molBr2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:

已知:转化过程中的反应为2CrO42-(aq)+2H+(aq)![]() Cr2O72-(aq)+H2O(l)。常温下Ksp[Cr(OH)3]=1×10-32。下列说法错误的是( )
Cr2O72-(aq)+H2O(l)。常温下Ksp[Cr(OH)3]=1×10-32。下列说法错误的是( )
A.反应①v正(CrO42-)=2v逆(Cr2O72-)时,反应处于平衡状态
B.反应②转移0.6mole-,则有0.2mol Cr2O72-被还原
C.除去废水中含铬离子的过程包括氧化还原反应和复分解反应
D.常温下,要使处理后废水中的c(Cr3+)降至1×10-5mol·L-1,反应③应调溶液pH=5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如图所示:
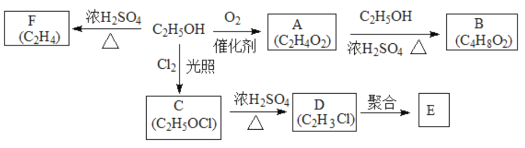
(1)A的结构简式为______。
(2)由A生成B的化学方程式为______。
(3)由乙醇生成C的反应类型为______。
(4)D中官能团名称是氯原子和______。
(5)由F生成乙醇的化学方程式为______。
(6)E的结构简式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关钠及其化合物的有关说法中正确的是( )
A.钠与CuSO4溶液反应的离子方程式为2Na+Cu2+═Cu+2Na+
B.7.8 g Na2O2含离子数为0.4NA
C.“侯氏制碱法”中的碱指NaHCO3
D.向Na2CO3饱和溶液中通入足量的CO2,有NaHCO3结晶析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化铝和氢氧化铝的叙述错误的是( )
A. Al(OH)3受热能分解
B. Al2O3既能溶于强酸溶液又能溶于强碱溶液
C. Al(OH)3胶体能吸附水中的悬浮物
D. Al(OH)3与过量的浓氨水反应生成NH4[Al(OH)4]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com